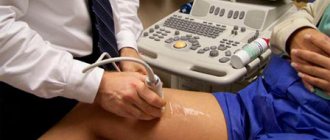
Замершая беременность – это патологический процесс, который характеризуется смертью плода во время внутриутробного развития. По статистике, подобное встречается практические в 20-25% всех беременностей, причем такая патология мало распространена среди пациенток в возрасте до 30 лет и встречается у каждой второй женщины старше 40-45 лет.
Прием акушера-гинеколога (врач высшей категории) 2 500 руб.
Прием врача-гемостазиолога 2 600 руб.
Все цены Записаться на прием
В нашей Международной клинике Гемостаза патология лечится опытными врачами-гинекологами, кандидатами и докторами медицинских наук. Наши специалисты имеют колоссальный опыт в диагностике, терапии и реабилитации подобных состояний. В результате даже после многократной замершей беременности нашим пациенткам удается забеременеть и выносить здорового малыша.
Когда и зачем нужен генетический анализ после замершей беременности
Главная цель исследования – выяснение причин остановки развития плода. На фоне повторяющихся выкидышей оно укажет факторы, провоцирующие привычное невынашивание беременности на раннем сроке.
Если не провести анализ ворсинок хориона после самоабортирования, ситуация может повториться при следующей беременности. Получив результаты цитогенетического анализа, доктор сможет выработать тактику лечения или предложит прибегнуть к услугам суррогатной матери.
Диагностическую значимость анализ имеет на сроке 10-12 недель, когда способность клеток к делению может быть сохранена. Врачи МЖЦ рекомендуют сдать анализы тем пациенткам, у которых замирание беременности констатировалось два и более раза:
- на раннем сроке;
- растёт ребёнок с болезнью Дауна, Эдвардса, другими пороками развития;
- имеются наследственные заболевания у родителей (в том числе по линии отца) ребёнка;
- установлены нарушения кариотипа, и диагностирована замершая беременность.
Почему замершая беременность опасна для женщины
Подобное состояние требует обязательного лечения, так как может привести к ряду серьезных осложнений. Среди них:
- Эндометрит (воспаление внутренней оболочки матки).
- Маточное кровотечение.
- Перитонит (воспаление брюшины).
- Сепсис тканей (генерализованный инфекционный процесс).
- Мацерация эмбриона (процесс внутриутробного разложения плода).
- Хориоамнионит (воспаление околоплодного пузыря).
Как видите, последствия действительно тяжелые и затрагивают разные системы организма. Отсутствие лечения может иметь самые неблагоприятные прогнозы для пациентки.
Как проводится исследование
Для цитогенетического исследования плода пригодно не только плодное яйцо, вышедшее после самоаборта, но и любой другой биоматериал, извлекаемый из матки при выскабливании. Кариотипирование возможно только при анализе живых клеток, поэтому при подозрении на хромосомные патологии, пациентке нужно находиться под постоянным наблюдением врача.
При замершей беременности важно не только вовремя получить материал, но и правильно его хранить и транспортировать. В нашем центре исследования проводятся в собственной лаборатории, поэтому проблема потери качества образца, как следствие – ошибки в установлении хромосомных патологий, не возникает.
Показания
Для исследования берется свежий образец тканей от выкидыша, для сравнительного анализа предоставляется кровь матери и отца. Правильно упакованные образцы с официальной формой-направлением отправляются в сертифицированную лабораторию, где проводится тестирование. Либо образцы можно сдать непосредственно в клинике, где имеется такая лаборатория. Продукты зачатия можно собрать в домашних условиях, если выкидыш случился дома, но чтобы правильно собрать материал, нужно получить подробные инструкции у своего врача.
До отправки в лабораторию сортировка образцов тканей не требуется, но это может существенно снизить вероятность контаминации. Сортировка включает удаление крупных сгустков крови из биоптата, тщательное промывание его физраствором пока не останется следов крови, отделение ворсин от оболочки и помещение их в чашу для образца.
Тестирование будет полезно женщинам с потерей беременности:
- старше 35 лет, с возрастом увеличиваются риски возникновения случайных хромосомных аномалий;
- с неоднократными выкидышами;
- после первого выкидыша, чтобы знать риски;
- имеющим детей с врожденными аномалиями;
- кто хочет узнать причину преждевременного прерывания беременности;
Также при планировании беременности лаборатория Natera предлагает:
| Тест | Что определяет | Когда проводится |
| PanoramaTM (не инвазивный пренатальный скрининговый тест, NIPT) | Несколько хромосомных анеуплоидий, определенные микроделеции | С 9 недель беременности |
| Horizon (скрининг на носительство) | Определяет риск передачи определенных генетических болезней последующим поколениям | До беременности или на ранних гестационных сроках |
| Vistara | Выявляет серьезные заболевания, связанные с 30 генами, которые стандартные НИПТ не исследуют. | С 9 недель беременности |
Кандидаты для биопсии эмбриона и ПГД
Кандидаты для биопсии эмбриона и ПГД включают в себя:
- Женщины старше 34 лет: женщины рождаются со всеми яйцеклетками, которые они будут когда-нибудь иметь, и по мере старения женщины ее яйцеклетки подвергаются также воздействию этого процесса старения. Таким образом, вероятность зачатия хромосомно аномального потомство с возрастом увеличивается. В целом риск анеуплоидии увеличивается с 1 на 385 в возрасте 30 лет, до 1 на 179 в возрасте 35 лет, до 1 на 63 в возрасте 40 лет, и в возрасте до 45 лет возможность рождения больного ребенка составляет 1 к 19. В результате использования ПГД при ЭКО стало известно, что в действительности больее чем 20% эмбрионов у женщин в возрасте от 35 до 39 анеуплоидны, и страдают почти 40% эмбрионов у женщин старше 40 лет. Большинство из этих эмбрионов в случае переноса в матку либо не имплантируются или приводят к невынашиванию. Это считается основной причиной низкой частоты наступления беременности и родов женщин в возрасте 40 лет и старше. До внедрения ПГД, для увеличения шансов на зачатие в матку переносилось большее число эмбрионов. По-прежнему настоятельно рекомендуется проведение пренатальной диагностики после цикла ЭКО, поскольку это подтверждает прогноз нормального потомства. Возможно также, что аномальные эмбрионы могут быть ошибочно определены как нормальные и перенесены в матку.
- Женщины с рецидивирующей потерей беременности (привычным невынашиванием): мужчина или женщина пары может иметь ненормальную упаковку хромосом, что может вызвать фатальные аномалии в некоторых беременностях, но не в других.
- Пары с транслокациями: транслокации – это изменения в конфигурации хромосом, при которых хромосомы прикрепляются друг к другу (робертсоновские) или участки разных хромосомах меняются местами (взаимные или реципрокные). Примерно 1 из 900 человек имеет робертсоновские транслокации с участием хромосом 13, 14, 15, 21, 22. Примерно 1 из 625 человек имеет взаимные транслокации. Для выявления наличия транслокаций может быть проведено кариотипирование обоих партнеров. Пары с транслокациями могут иметь периодические потери беременности, или потомство с психическими или физическими проблемами. При сбалансированной транслокации, когда нет дополнительного или отсутствия хромосомного материала, и разрыв в хромосоме не нарушает функции генов, человек не страдает. Носители сбалансированных транслокаций могут быть затронуты сложными врожденными пороками развития, которые могут или не могут быть связаны с наследственным заболеванием. При несбалансированной транслокации, при которой существует или отсутствует дополнительный материал хромосом, отдельные личности, как правило, не будут затронуты, хотя у некоторых будет наблюдаться снижение фертильности. Однако существует риск того, что яйцеклетки или сперматозоиды от такого человека могут иметь несбалансированные транслокации, в результате чего эмбрион будет несбалансированным. Это может привести к неудаче имплантации, повторному невынашиванию, или потомству с психическими или физическими проблемами.
- Пары с аутосомно-доминантными заболеваниями, при которых будут затронуты 50% эмбрионов. Пары, которые имеют данные нарушения в семейном анамнезе, или являются носителями, или страдают от наследуемых заболеваний.
Пары с повторными неудачами ЭКО.
- Пары с историей бесплодия могут быть в состоянии определить этиологию, и, следовательно, выбрать соответствующее лечение.
- Парам из группы риска для наследования потомством болезни с угрозой для жизни, болезни с поздним началом (болезнь Хантингтона), предпочтительно планировать, выбрать соответствующие методы лечения, или ускорить процесс диагностики (например, ранней диагностики рака молочной железы)
- Пары, желающие потомство для производства HLA-совпадающих стволовых клеток, для страдающего ребенка со смертельным заболеванием.
Используемые методы
Для анализа на наличие генетических дефектов эмбриона, из него необходимо удалить либо первое полярное тельце из неоплодотворенной яйцеклетки и/или 1 или 2 клетки от каждого эмбриона. Это называется биопсией яйцеклетки или эмбриона и обычно делается перед тем, как происходит оплодотворение, или через 3 дня после оплодотворения. Биопсия на 6-10 клеточной стадии не оказывает отрицательного влияния на преимплантационное развитие. На этом этапе каждая клетка имеет полный набор хромосом. Обычно из эмбриона удаляется только одна клетка, так как ожидается, что будут одинаковыми со всеми другими клетками в эмбрионе. Иногда необходимо удалить вторую клетку из эмбриона, например, если сигнал в первой не обнаружен. Для диагноза предрасположенности с помощью первого и второго полярных телец, как показателей генетического статуса яйцеклетки, используется анализ методом FISH. Недостатком анализа полярных телец заключается в том, что он не принимает во внимание отцовские анеуплоидии.
Анализ биопсированной клетки использует один из двух методов:
- Флуоресцентная гибридизация in situ (FISH): биопсированная клетка фиксируется на предметном стекле, нагревается и охлаждается, и ее ДНК «помечается» цветными флуоресцентными красителями, называемыми зондами (маленькие кусочки ДНК, которые соответствуют исследуемым хромосомам), по одному для каждой определяемой хромосомы. В настоящее время может быть идентифицировано 8 из 23 хромосом. После завершения эмбриолог учитывает цвета под мощным микроскопом и в состоянии, в большинстве случаев, отличить нормальные от аномальных клеток. Этот процесс занимает около суток. Нормальные эмбрионы будут либо перенесены в матку на 4-й день после поиска яйцеклеток, или подвергнутся продленному культивированию и будут перенесены на 5-й день, как бластоцисты. Клетки, использовавшиеся для ПГД, больше не жизнеспособны, и не будут возвращены в эмбрион, но могут быть сохранены для будущих исследований.
- Полимеразная цепная реакция (ПЦР): методика, которая увеличивает количество копий специфичных регионов ДНК, чтобы произвести достаточное для анализа количество ДНК. ДНК является двухцепочечной (за исключением некоторых вирусов), и две цепи соединяются очень специфическим образом. «Последовательность кирпичиков» генов представляет собой определенный порядок появления 4-х различных дезоксирибонуклеотидов в сегменте ДНК. Эти 4 компонента: аденин (А), тимидин (T), цитозин (C), и гуанин (G). Последовательность этого 4-буквенного алфавита генерирует состав гена. При этой методике ДНК нагревают (денатурируют), чтобы разделить 2 нити. Далее добавляются праймеры и ДНК охлаждается, с тем чтобы опять образовались двойные нити. Затем в циклы добавляют ферменты, которые могут «прочитать» последовательность гена, что приводит к умножению ДНК. ПЦР используется для диагностики ген-специфических заболеваний, так же как и для выявления болезнетворных вирусов и/или бактерий, или в криминалистике в связи с подозрением в совершении преступления.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Определение хромосомных причин молярной беременности
Состояние, при котором эмбрион не развивается нормально, а ворсины хориона образуют пузыри с жидкостным содержимым называется пузырным заносом или молярной беременностью. Встречаемость данного редкого осложнения примерно 1:1000–5000 беременных. Больше рискуют женщины, забеременевшие после 40-летнего возраста, с предыдущим выкидышем или молярной беременностью, у которых имеется недостаток бета-каротина.
Пузырный занос представляет большую угрозу здоровью и жизни женщины. Он бывает полным (80% случаев), характеризуется отсутствием эмбриональной ткани и неполным. Причиной полного заноса является оплодотворение женской половой клетки, не содержащей хромосом. При дальнейшем мейозе отцовский хромосомный набор удваивается, при этом только растут хорионические ворсины, а сам зародыш так и не образуется.
Неполный пузырный занос обусловлен оплодотворением женской гаметы двумя спермиями, при этом появляются лишние хромосомы, а продукт зачатия становится нежизнеспособным. Причиной является триплоидия мужского происхождения. При данном состоянии ткани продукта зачатия стимулируют выработку хорионического гонадотропина. Высокий уровень ХГЧ способствует образованию лютеиновых кистозных образований в яичниках. 15–20% случаев молярной беременности осложняются развитием злокачественного новообразования: при внедрении продуктов зачатия в здоровые материнские ткани развивается хорионэпителиома.
Пузырный занос нужно удалять хирургическим путем, после чего проводить контроль ХГЧ. При хорионэпителиоме проводится операция и химиотерапия. Решающее значение для пациентки имеет своевременное обнаружение молярной беременности. УЗИ поможет только выявить пузырный занос, тест Анора позволит определить происхождение триплоидии. Это единственное тестирование, позволяющее обнаружить причину пузырного заноса и предотвратить развитие у женщины трофобластической болезни.
С помощью тестирования Анора количество проанализированных образцов составляет 7549, из них хромосомные отклонения в 1268 образцах имеют фетальное происхождение, в 1201 образцах – с контаминацией. 95% женщин, переживших выкидыш и воспользовавшиеся тестом Анора, были удовлетворены результатами, поскольку узнали причины невынашивания и могли тщательнее подготовиться к следующей беременности. Две трети пациентов, которые не воспользовались возможностью пройти тестирование, хотели бы сделать хромосомный анализ.
Как передаются по наследству генетические заболевания
В диаграммах ниже, D или d представляет дефектный ген, а N или n представляет нормальный ген. Мутации не всегда приводят к болезни.
Доминантные заболевания:
Один из родителей имеет один дефектный ген, который доминирует над своей нормальной парой. Так как потомки наследуют половину своего генетического материала от каждого из родителей, есть 50% риск наследования дефектного гена, и, следовательно, заболевания.
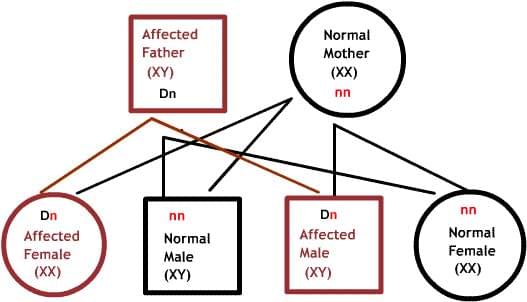
Рецессивные заболевания:
Оба родителя являются носителями одного дефектного гена, но при этом имеют нормальную пару гена. Для наследования заболевания необходимы две дефектных копии гена. Каждый потомок имеет 50% шанс быть носителем, и 25% шанс унаследовать заболевание.
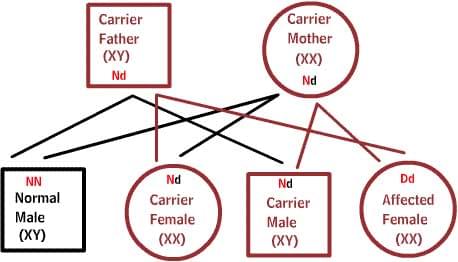
X-сцепленные заболевания:
Нормальные женщины имеют XX хромосомы, а нормальные мужчины XY. Женщины, которые имеют нормальный ген на одной из Х-хромосом, защищены от дефектного гена на их другой Х-хромосоме. Однако, у мужчины отсутствует такая защита в связи с наличием только одной Х-хромосомы. Каждый мужской потомок от матери, которая несет в себе дефект, имеет 50% шанс унаследовать дефектный ген и заболевание. Каждый женский потомок имеет 50% шанс быть носителем, как и ее мать. (на рисунке ниже X представляет нормальный ген а X представляет дефектный ген)
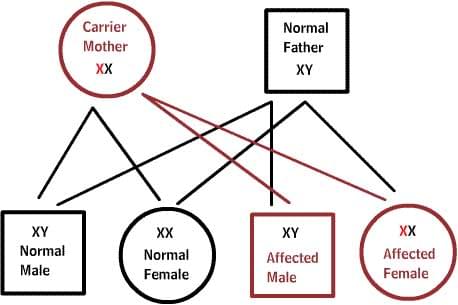
История преимплантационной генетической диагностики (ПГД)
Первые живорождения после ПГД были зарегистрированы в Лондоне в 1989 году. Две двойни девочек-близнецов родились от пяти пар с риском передачи связанного с Х-хромосомой заболевания. В настоящее время с помощью методов генетического анализа или ПГД могут быть обнаружены около 90% аномальных эмбрионов. Не все хромосомные или генетические заболевания могут быть определены этими процедурами, так как в ходе одной процедуры может быть диагностировано только ограниченное число хромосом. Многочисленные исследования на животных и некоторые исследования на человеке показывают, что микрохирургия эмбриона (биопсия), необходимая для удаления клеток, не влияет на нормальное развитие ребенка. Эта процедура, однако, была выполнена относительно небольшому числу пациентов во всем мире, поэтому точные негативные последствия, если таковые имеются, неизвестны. Несмотря на то, что после генетического анализа для выявления анеуплоидии всем мире на сегодняшний день было рождено уже много детей, эта процедура все еще относительно нова. В исследованиях на животных не было обнаружено никаких очевидных проблем и предварительные данные с эмбрионами человека позволяют предположить справедливость этого вывода. В исследовании, проведенном в Университетском колледже Лондона, исследователи недавно рассмотрели 12 преимплантационных эмбрионов с новой техникой, которая сочетает в себе амплификацию всего генома (WGA) и сравнительную гибридизацию генома (CGH). В результате в 8 из 12 изученных эмбрионов были обнаружены значительные хромосомные аномалии. Это может объяснить, почему люди имеют в лучшем случае 25% шансов на достижение жизнеспособной беременности в месяц при естественном зачатии.