Лейкопения
Диагноз «лейкопения» означает низкий уровень белых кровяных телец – лейкоцитов, являющихся важным элементом иммунной системы (медики называют их иммунокомпетентными клетками). У взрослых людей граничным считается показатель 4000 лейкоцитов на 1 микролитр крови. У детей пороговое значение рассчитывается индивидуально с учётом возраста.
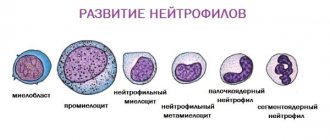
Специалисты различают несколько разновидностей лейкопении в зависимости от того, каких белых кровяных телец недостаточно (лимфоцитов, нейтрофилов, моноцитов и т.д.). Чаще всего диагностируется дефицит нейтрофилов, на которые возлагается защита организма от бактериальных и грибковых инфекций, в этом случае ставится диагноз нейтропения. На втором месте по частоте случаев – недостаток лимфоцитов, обеспечивающих защиту от вирусных заболеваний.
Лейкопения у ребенка: причины
Низкое количество белых кровяных клеток обычно означает, что организм не производит белых кровяных клеток в достаточно количестве. Важно помнить, что это может увеличить риск развития всевозможных инфекций.
Общие причины, которые вызывают низкий уровень лейкоцитов в крови, следующие:
- Лечение раковых заболеваний посредством лучевой терапии.
- Прием антипсихотических препаратов.
- Прием лекарств для снижения активности щитовидной железы.
- Развитие инфекционных заболеваний, таких как ВИЧ или гепатит.
- Аутоиммунные расстройства, такие как ревматоидный артрит.
Некоторые категории населения, имеющие афро-карибское и ближневосточное происхождение, часто более склонны к низкому уровню лейкоцитов. Также иногда по наследственности передается низкое количество лейкоцитов в крови. Подобные случаи считаются нормальными и не увеличивают риск заражения, поэтому медикаментозная коррекция не требуется.
Видео: Клинический анализ крови — Школа доктора Комаровского
Причины развития лейкопении
Снижение числа белых кровяных телец в русле крови может быть связано с тремя основными причинами:
- Нарушение процесса образования лейкоцитов. Последние продуцируются в зобной железе (тимусе), лимфоузлах, селезёнке, миндалинах, лимфоидных узелках кишечника и тканях костного мозга – проблемы в работе любого из этих органов могут повлечь за собой нарушения выработки кровяных телец.
- Разрушение лейкоцитов.
- Нарушение циркуляции лейкоцитов в тканях организма.
Перечисленные нарушения могут быть вызваны наследственными факторами. Это врождённые патологии, нарушающие функции костного мозга, такие как синдром Костмана – в подобных случаях говорят о первичной лейкопении, что встречается достаточно редко. Более распространённый вариант – вторичная (приобретённая) лейкопения. Один из самых частых факторов, вызывающих развитие лейкопении — лучевая или химиотерапия, вследствие которой нарушается процесс выработки зрелых лейкоцитов. Однако есть и другие причины:
- Аутоиммунные нарушения, сопровождающиеся разрушением клеток костного мозга и/или лейкоцитов.
- Болезни крови (острые лейкозы, анемии).
- Вирусные инфекции, истощающие запасы лейкоцитов (организм не успевает воспроизводить новые кровяные тельца).
- Приём ряда лекарственных препаратов. В их число входят антибиотики, цитостатики, противовоспалительные средства (типа анальгина), а также противосудорожные препараты, нейролептики и др.
- Действие токсических веществ, таких как угарный газ, ртуть, свинец.
- Действие негативных физических факторов, например, ионизирующее излучение.
Лейкопения нередко сопровождает следующие заболевания:
- ВИЧ-инфекция;
- туберкулёз;
- системные васкулиты;
- болезни суставов (ревматоидный артрит и др.);
- воспалительные заболевания кишечника (болезнь Крона и др.);
- рассеянный склероз;
- эндокринные расстройства.
Снижение числа лейкоцитов также может наблюдаться после переливания крови и при белковом голодании (недоедание, недостаток витаминов).
У детей наиболее частые причины развития вторичной лейкопении – такие инфекционные болезни, как грипп, корь, свинка (паротит).
Медицинские интернет-конференции
Ранняя диагностика онкогематологических заболеваний у детей чрезвычайно сложна ввиду неспецифичности первичных симптомов, которые часто скрываются под «масками» других заболеваний [2, 27]. Онкологическая настороженность и знание вероятных симптомов позволит практическому врачу раньше диагностировать данную патологию и, следовательно, существенно улучшить прогноз для больного [1, 3, 4, 5].
У большинства детей острый лимфобластный лейкоз (ОЛЛ) манифестирует бурно и характеризуется полиморфизмом клиники. Стадия предлейкоза не имеет характерных клинических симптомов [6, 7], а анализ симптомов начального периода проводится ретроспективно [7], в связи с чем, диагноз не бывает поставлен вовремя. Несмотря на прогресс лабораторной диагностики, выявить лейкоз у детей на ранних этапах сложно, т.к. для появления характерных изменений гемограмме опухоль должна достичь критической массы [4], а манифестация ОЛЛ связана с бластной инфильтрацией различных органов с нарушением их функции [8]. Клиническая симптоматика в данном случае опережает лабораторные изменения, и ребенок не госпитализируется в специализированный гематологический стационар [55].
ОЛЛ встречается преимущественно у детей от 0-15 лет, при этом в возрасте 2-5 лет наблюдается пик заболеваемости [54]. Более благоприятный прогноз и эффект от проводимой терапии наблюдается у детей от 1 до 10 лет, в то время как у детей младше 1 года и старше 10 лет ОЛЛ протекает неблагоприятно и трудно поддается лечению [46].
Гендерные различия:
Исследования, направленные на изучение межполовых различий при ОЛЛ показали, что при В-ОЛЛ распределение по полу было одинаковым: мальчики — 51%, девочки — 49 %, а то время как Т-вариант обнаруживался преимущественно у мальчиков (90 %).
Конституциональные особенности. В литературе имеются данные о связи дебюта и течения начального периода ОЛЛ с конституциональным типом ребенка (астеноидный, торакально-мышечный, дигестивный): наиболее тяжелое течение наблюдается у детей с дигестивным типом телосложения [55].
Предрасполагающие факторы. В диагностике ОЛЛ врач должен учитывать и большой спектр предрасполагающих факторов, которые могут привести к развитию ОЛЛ: социально-экономический статус семьи ребенка, хромосомные аномалии, синдром Дауна, нейрофиброматоз, вариабельный иммунодефицит, дефицит Ig А, анемия Фанкони, синдром Швахмана, врожденная Х-сцепленная агаммаглобулинемия [56].
В клинической картине острого лимфобластного лейкоза наиболее часто встречаются 5 основных синдромов (таблица 1):
- Интоксикационный синдром. Наиболее часто больных беспокоит длительная лихорадка неясного генеза, интоксикация различной степени, слабость, лихорадка, недомогание, потеря массы тела. Лихорадка может быть связана и с наличием бактериальной, вирусной, грибковой или протозойной (реже) инфекцией, особенно у детей с нейтропенией [7].
- Костно-суставной синдром. Проявления со стороны опорно-двигательного аппарата выявляются преимущественно у детей с В-клеточным ОЛЛ, который характеризуется меньшим вовлечением экстрамедуллярных органов и нечеткими изменениями в периферической крови [18]. Костно-суставной синдром часто является первым проявлением ОЛЛ у детей [9, 10]. Проведенные исследования показали, что у пациентов с ОЛЛ в 54% случаев регистрировался костно-суставной синдром, с более высокой частотой у детей от 1 до 9 лет. Наличие болезненности суставов отмечалось у 16,2% детей с ОЛЛ, артрит – у 26,6%, изменение походки у 32,8%. Чаще поражались крупные суставы: коленные — 10,6%, голеностопные — 9,4%, локтевые — 4,4%, плечевые — 3,6% [11]. При осмотре выявлялась отечность суставов, наличие выпота и нарушение функции пораженной конечности [12]. Нередко больные предъявляли жалобы на частые и множественные переломы, в основе которых могут лежать явления остеопороза [13]. Также необходима уточняющая диагностика при подозрении на рецидивирующий мультифокальный остеомиелит [14]. Острый лимфобластный лейкоз в редких случаях проявляется остеоартритом, неправильная интерпретация которого может привести ошибкам в дифференциальной диагностике с ювенильным ревматоидным артритом (ЮРА). У детей с ОЛЛ отмечается асимметричный олигоартрит, который проявляется лихорадкой, бледностью, артритом, ночными болями, болями в костях [19]. Для поражения костной системы в дебюте ОЛЛ характерен полиморфизм рентгенологических проявлений. В одних случаях они малоинформативны (выявляется лишь незначительная периостальная реакция) [15], в других случаях выявлялись остеолиз, остеопения, остеосклероз, патологические переломы, периостальные реакции и смешанные поражения в виде лизис-склероза [16]. Важным симптомом является несоответствие клинической симптоматики рентгенологическим данным. Сочетание гипертермии, интоксикационного и суставного синдромов может имитировать септический артрит. Однако отсутствие адекватного ответа на антибактериальную терапию позволяет заподозрить ОЛЛ. Патологический процесс в данном случае развивается вследствие метафизарного склероза [3]. Некупируемые болевой и суставной синдромы, характерные для ювенильного идиопатического артрита, необходимо рассматривать с позиций дифференциальной диагностики с ОЛЛ [16]. Подобная клиническая симптоматика в сочетании с панцитопенией характерна для некроза вещества костного мозга [17]. Эти данные подчеркивают важность включения ОЛЛ в дифференциальную диагностику нарушений опорно-двигательного аппарата даже при явно нормальной картине периферической крови.
- Лимфопролиферативный синдром. Увеличение лимфатических узлов связано с лейкозной инфильтрацией тканей [57]. Наиболее часто увеличиваются шейные, паховые, подмышечные лимфатические узлы, которые имеют плотноэластическую консистенцию, при пальпации безболезненны, не спаяны с окружающей клетчаткой, подвижны, кожа над ними не изменена. У некоторых детей может наблюдаться симптомокомплекс Микулича (одновременное увеличение лимфатических узлов в подчелюстной, околоушной и окологлазничной области). Возможно значительное увеличение лимфоузлов средостения вплоть до сдавления верхней полой вены (одышка, цианоз, одутловатость лица, пастозность век, выбухание шейных вен). Наряду с лимфоаденопатией в 75% случаев выявляется гепатоспленомегалия, которая не сопровождается болевым синдромом [2, 6].
- Анемический синдром характеризуется нарастающей бледностью при ухудшении общего состояния, головокружениями и головной боль, одышкой, тахикардией [2].
- Геморрагический синдром связан как с тромбоцитопенией, так и с внутрисосудистым тромбозом (особенно при гиперлейкоцитозе) [46]. Больные могут предъявлять жалобы на полиморфные кровоизлияния (от петехий до кровоизлияний крупных размеров) на коже и в подкожножировой клетчатке различной локализации. Наблюдаются кровотечения из слизистых оболочек (носовые, десневые, желудочно-кишечные, почечные, маточные) [2, 58].
В клинике могут наблюдаться, а в ряде случаев и преобладать [27], клинические проявления со стороны других органов (таблица 1).
- Поражения слизистых оболочек. Одним из ранних симптомов ОЛЛ у детей являются поражения слизистой оболочки полости рта в виде эритемы, язв и отека губ, языка, неба и десен [21]. Нередко постановка диагноза сопровождается трудностями в дифференциальной диагностике с хирургической патологией лица. Так, описан случай ОЛЛ у девочки с отеком носогубной области, который был расценен как флегмона. Вышеописанные изменения были связаны с инфильтрацией слизистой оболочки и мягких тканей бластными клетками [22].
- Кожные проявления. ОЛЛ у детей в некоторых случаях манифестирует в виде различных кожных проявлений, в основе которых лежит, как правило, лейкозный инфильтрат с поражением кожи и подкожных тканей. Локализация может быть различна: поражается область головы в виде небольших узелков [23], либо другие участки кожи [24]. Описан случай поражения кожи наружного слухового прохода, при котором ребенку первоначально был выставлен диагноз «Диффузный наружный отит» [25].
- Поражения глаз. Офтальмологические проявления у больных, страдающих острым лимфобластным лейкозом, могут быть и его первым проявлением [26, 27]. Жалобы и клинические проявления при этом отличаются полиморфизмом [28]. Наиболее частым признаком поражения глаз при ОЛЛ являются кровоизлияния в различные отделы глазного яблока: сетчатку, субконьюнктивальные кровоизлияния [29]. При осмотре глазного дна может выявляться отек соска зрительного нерва и инфильтрация сосудов.
- Абдоминальный синдром. Абдоминальный синдром проявляется в виде болей в животе неясной этиологии, чередования поносов и запоров, что связано с лимфоидной инфильтрацией паренхиматозных органов и стенки кишечника. В редких случаях ОЛЛ может скрываться под «маской» острого панкреатита, который плохо поддается лечению [30], а также тифлита [31], что требует дополнительной дифференциальной диагностики.
- Поражение мочеполовой системы. Клинические проявления заболеваний почек, вызванные злокачественной инфильтрацией, могут быть первичным проявлением заболевания у пациентов с ОЛЛ и представлены острой почечной недостаточностью [32, 33], ренальной артериальной гипертензией [34], синдромом пальпируемого образования и двухстронней нефромегалией, которые необходимо дифференцировать с опухолью Вильмса [35, 36]. Особенностью клиники ОПН в таких случаях является отсутствие олигурии на фоне выраженной нефромегалии [37, 38]. Кроме того, имеются данные о первичном проявлении ОЛЛ в виде ночного энуреза у ребенка [39].
- Неврологическая симтоматика. Неврологическая симптоматика является не только признаком развития нейролейкемии у детей с ОЛЛ, но может быть и единственным ранним клиническим проявлением заболевания. Клиническая картина преимущественно связана с поражением черепно-мозговых нервов (ЧМН). В одном из случаев при поражении двигательной ветви тройничного нерва у ребенка единственным симптомом являлся тризм жевательной мускулатуры [40], а в другом, при поражении чувствительной ветви, отмечалась сенсорная нейропатия (Numb chin syndrome) [41]. Первичным проявлением ОЛЛ в ряде наблюдений явилось изолированное поражение отводящего нерва с соответствующими глазодвигательными симптомами [42, 43]. Помимо поражения ЧМН в клинике могут наблюдаться и проявления нейродегенерации (атаксия-телеангиоэктазия Луи-Бар) с соответствующими иммунными и гематологическими нарушениями [44]. ОЛЛ может дебютировать в виде паранеопластического неврологического синдрома (ПНС), проявляющегося острой мышечной слабостью проксимальных мышц верхних и нижних конечностей [20].
- Поражение легких. Нарушения дыхательной системы могут быть связаны с увеличенными лимфоузлами средостения, характерными для Т-клеточной лейкемии, приводящими к развитию синдрома верхней полой вены или дыхательной недостаточности. Могут быть лейкемическая инфильтрация легочной ткани и/или кровоизлияния в нее. Иногда сложно дифференцировать эти осложнения с инфекционным процессом [45].
- Нарушения минерального обмена. Развивающиеся при ОЛЛ нарушения минерального обмена характеризуются гиперкальциемией, которая может быть первым симптомом заболевания [50, 51], либо его осложнением [52]. У пациентов с гиперкальциемией превалируют жалобы со стороны ЖКТ и костно-суставной системы [53].
- Инфекционные заболевания. В ряде случаев дебют ОЛЛ может протекать под «маской» некоторых инфекционных заболеваний, например, острая респираторная вирусная инфекция, инфекционный мононуклеоз, ангина, коклюш, паракоклюш, пневмония, эпидемический паротит [59, 60, 61, 62].
Гематологические изменения. Важнейшим диагностическим исследованием, позволяющим предположить ОЛЛ, является общий клинический анализ крови с подсчетом лейкоцитарной формулы.
Гематологические сдвиги при ОЛЛ не имеют четких закономерностей, и часто их выраженность может не соответствовать клинической симптоматике, изменения в анализе крови, характерные для ОЛЛ, могут отсутствовать, что указывает на проведение комплексной оценки клинических и лабораторных данных.
Наиболее часто в гемограмме выявляется выраженный лейкоцитоз, при этом количество лейкоцитов варьирует в широких пределах и зависит от варианта ОЛЛ. Так, среднее количество лейкоцитов у детей с В-варианте ОЛЛ составило 37,1 ± 12,2*109/л, при Т-варианте ОЛЛ – 123,3 ± 36,5*109/л [63]. Отмечается, что формы ОЛЛ с гиперлейкоцитозом прогностически более неблагоприятны [46].
Наряду с лейкоцитозом, наблюдается бластемия до 80-90% [27], причем небольшой процент бластных клеток не дает оснований для постановки диагноза ОЛЛ, в то время как и их отсутствие не позволяет полностью его исключить [47, 64].
В редких случаях в дебюте заболевания отмечается стойкая необъяснимая гиперэозинофилия (до 80%), которая может сочетаться с кожными проявлениями [48], а в 25-30% случаев — лимфоцитоз. Для цитопенического варианта ОЛЛ характерна лейкопения и абсолютная нейтропения [4]. Увеличение лейкоцитарного пула приводит к угнетению других ростков кроветворения, что сопровождается снижением количества эритроцитов и гемоглобина, а также тромбоцитопенией [27, 46, 65, 66].
В ряде работ имеются данные о развитии метаболического лактоацидоза в начальном периоде ОЛЛ [49].
Таким образом, первичные клинические проявления острого лимфобластного лейкоза у детей характеризуются выраженным полиморфизмом, что требует от врачей всех специальностей онкологической настороженности, комплексной оценки анамнеза, последовательного анализа клинических данных со стороны всех систем организма, применение адекватного комплекса лабораторно-инструментальных исследований. В сомнительных случаях ребенок должен быть направлен на консультацию к детскому гематологу-онкологу.
Симптомы
Часто лейкопения обнаруживается случайно, например, во время профилактических медицинских осмотров, поскольку человек может длительное время не замечать никаких нарушений. Первыми признаками лейкопении могут быть:
- головные боли;
- головокружения;
- ощущение слабости;
- учащённое сердцебиение;
- кровоточивость дёсен, язвы в полости рта;
- осиплый голос.
При прогрессировании патологии наблюдаются:
- повышение температуры тела;
- лихорадка, озноб;
- увеличение миндалин и селезёнки;
- истощение организма.
Высокая восприимчивость к инфекционным заболеваниям – ещё один симптом, который может говорить о лейкопении.
В зависимости от числа лейкоцитов различают три стадии патологии: первая (менее 1,5 г/л), вторая (1 г/л) и третья (0,5 г/л). На третьей, самой тяжёлой стадии, получившей название агранулоцитоз, может развиться тромбоцитопения – патология, характеризующаяся уменьшением числа тромбоцитов, что грозит кровотечениями и кровоизлияниями.
Агранулоцитоз — тяжелая патология, при которой резко снижается количество лейкоцитов и гранулоцитов. Поскольку гранулоциты обеспечивают противомикробную защиту организма, критическое уменьшение их количества может привести к серьезным инфекционным осложнениям вплоть до летального исхода. Больному с таким диагнозом назначается госпитализация и неотложное лечение в гематологическом отделении, с обязательным созданием асептических условий.
Острая лейкопения может длиться до трёх месяцев, при более длительных сроках ставится диагноз хроническая лейкопения.
Лейкопения у детей: симптомы
Симптомы зависят от типа количественного изменения лейкоцитов у ребенка. Общие признаки состояния, когда лейкоцитов слишком мало или они не функционируют должным образом, представляют собой следующее:
- Частые инфекционные заболевания, в основном поражаются легкие, уши или придаточные пазухи.
- Абсцессы кожных покровов.
- Язвы в ротовой полости.
- Инвазивные грибковые заболевания.
- Тяжелые поражения зубов и десен (пародонтоз).
Краткая клиническая характеристика:
- Ушные воспалительные заболевания вызывают боль в пораженном ухе.
- Инфекции придаточных пазух могут вызвать головную боль, затрудненное дыхание или кашель.
- Пневмония — это воспаление легких, которое может вызвать озноб, кашель, одышку и мышечные боли.
- Инфекционное воспаление мочевого пузыря нередко становится причиной жара, тошноты или боли при мочеиспускании.
Некоторые нарушения могут проявляться уникальными симптомами, такими как:
- Замедление заживления ран при дефиците адгезии лейкоцитов.
- Хроническая, иногда жировая, диарея, что характерно для синдрома Швахмана-Даймонда.
Менее характерными признаками считается слабость, быстрая утомляемость, головокружение, озноб и дрожь, но их появлением не стоит игнорировать. Если у ребенка имеются даже обычные симптомы простуды, стоит обратиться к лечащему педиатру. При необходимости врач направит к гематологу для проведения дальнейших исследований, а в случае надобности назначит лекарства.
Дефиците адгезии лейкоцитов
Диагностика
Поставить точный диагноз помогают клинические исследования элементов крови. Назначить необходимые исследования может врач-терапевт. Для определения уровня лейкоцитов необходимо сдать венозную или капиллярную кровь утром натощак.
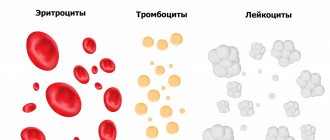
В первую очередь проводят гемограммы для подсчёта количества разных видов кровяных телец (эритроцитов, лейкоцитов и т.д.) и определения их процентного соотношения. Для определения типа лейкопении и причины ее возникновения назначают цитологические исследования. Комплексная диагностика также включает биохимический и иммунологический анализы крови, а также анализ крови на гепатит. В каждом случае полный список необходимых лабораторных исследований устанавливается с учётом анамнеза конкретного пациента.
Лечение
Схема и препараты для лечения лейкопении подбираются в зависимости от того, уровень каких именно кровяных клеток опустился ниже нормы и что послужило причиной этому. Как правило, пациенту назначается комбинированная терапия, которая подразумевает приём медикаментов, специальную диету и изменение образа жизни.
Стандартное лечение включает приём средств:
- улучшающих метаболизм;
- увеличивающих число нейтрофильных гранулоцитов;
- стимулирующих активность стволовых клеток костного мозга других клеток, принимающих участие в выработке лейкоцитов.
Поскольку чаще всего лейкопения выступает в качестве вторичной патологии, в первую очередь важно устранить первопричину:
- Если лейкопению спровоцировал приём лекарственных препаратов, может быть принято решение об их срочной отмене или замене.
- Если дефицит кровяных телец — это следствие какого-либо заболевания, нужно прежде всего заняться его лечением. Так, чтобы добиться ремиссии при аутоиммунных нарушениях, используют иммуносупрессанты и глюкокортикостероиды. В случае онкогематологической патологии назначают химиотерапевтические препараты. Пациентам с бактериальными инфекциями выписывают антибиотики и т.д.
- В случае генетических отклонений, а также пациентам, принимающим химиотерапию, дополнительно назначают приём факторов роста (белков), стимулирующих выработку лейкоцитов.
Помимо медикаментозного лечения, нужно:
- Нормализовать рацион, добавив в меню продукты, богатые витаминами и минералами, в частности овощи и фрукты. Врач дополнительно может назначить при диагнозе лейкопения витамины В6, В2, В12, а также фолиевую кислоту и др.
- Обеспечить полноценный отдых.
- Создать асептические условия. Важно соблюдать санитарно-гигиенические нормы и избегать травм (порезов, царапин), через которые в организм может проникнуть инфекция.