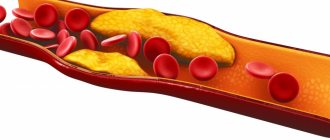
Несмотря на то что о холестерине человечество узнало еще в 18 веке, говорить активно о нем стали в конце 90-х. С появлением анекдота о том, что сало — это чистый холестерин убитого животного мы стали ассоциировать этот термин с чем-то плохим или прямой угрозой для нашего здоровья. На сегодняшний день часто приходится слышать “У меня высокий уровень холестерина” или “Нужно проверить холестерин”. Давайте попробуем разобраться что такое холестерин и нужно ли его бояться.
Холестерин — это жироподобное вещество, которое нам необходимо для:
- Создания здоровых клеток (мембран эритроцитов, мембран клеток печени, мозга (серого и белого вещества)
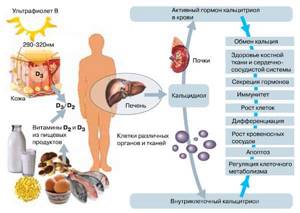
- Нормального пищеварения (холестерин нужен для выработки холевых или желчных кислот, которые расщепляют жир и жирорастворимых витаминов (например витамина D)
- Синтеза гормонов (тестостерона, эстрогена, прогестерона и даже кортизола)
- Синтеза витамина Д
- Работы иммунной, репродуктивной, нервной систем и в целом нормальной жизнедеятельности организма.
Где берется холестерин?
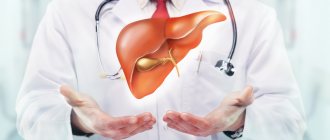
Источниками холестерина являются частично продукты, которые мы потребляем (около 20% от всего количества холестерина в организме). Но основной процент вещества синтезируется в печени, которая ответственна за выработку 80% эндогенного холестерина. Другими участками синтеза, но в значительно меньшей степени являются кора надпочечников, яичек, яичников и кишечник.
Печень синтезирует холестерин для экспорта в другие клетки, и также способствует удалению избыточного холестерина из организма. Это достигается путем преобразования холестерина в соли желчи и переноса в желчь, из которой он в конечном итоге и выводится. Кроме того, печень синтезирует большинство необходимых липопротеинов, необходимых для транспортировки холестерина по всему организму. Так как холестерин переносится через кровь, но имея жироподобную структуру не растворяется в ней, а присоединяется к белкам, которые действуют как его носители. Комбинация белков и холестерина называется липопротеидами.
Синтез и разрушение липидов
В процессе пищеварения, мы потребляем жиры, белки и углеводы. Основным местом сбора и последующей переработки жиров является печень. В ней образуются липопротеины и холестерин. Весь холестерин, который не используется клетками, возвращается в печень и опять перерабатывается. Если эти метаболические процессы находятся в равновесии, стенки артерий остаются чистыми и эластичными, если эти метаболические процессы нарушены, уровень липидов в крови изменяется, стенки артерий повреждаются и теряют гладкость и упругость.
Липопротеиды высокой (ЛПВП) и низкой (ЛПНП) плотности или «плохой» и «хороший холестерин»
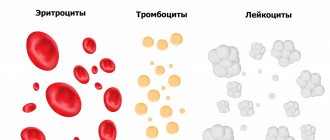
Существуют несколько важных типов липопротеидов, ответственных за перемещение холестерина. Основные это:
- Липопротеиды низкой плотности (ЛПНП), которые перемещают холестерин из печени в другие клетки организма. Их часто называют «плохим холестерином». Они переносят частицы холестерина по всему телу и могут накапливаться на стенках повреждённых сосудов, делая их менее эластичными и сужеными.
- Липопротеиды высокой плотности (ЛПВП) или «хороший» холестерин, которые поглощают избыток холестерина в организме и транспортируют его в печень для выведения с желчью. Эти липопротеиды хорошо растворимы и не склонны к выделению холестерина в осадок на стенках сосудов (то есть не способствуют образованию атерогенных бляшек).
Часто, когда говорят о высоком уровне холестерина, имеют в виду повышенный уровень холестерина липопротеидов низкой и очень низкой плотности ЛПНП (ЛПНП-Х). Когда уровень ЛПНП увеличивается, повышается риск сердечно-сосудистых заболеваний.
| Холестерин липропотеидов низкой плотности (ЛПНП) или «плохой холестерин» | Холестерин липопротеидов высокой плотности (ЛПВП) или хороший холестерин | Холестерин липопротеидов очень низкой плотности (пре-бета липротеиды), триглицериды |
|
|
|
Контроль над уровнем “плохого” холестерина является важной частью снижения риска развития сердечных заболеваний, сердечного приступа или инсульта.
При повышении уровня холестерина могут развиваться жировые отложения в кровеносных сосудах. Со временем эти отложения растут, что затрудняет прохождение достаточного количества крови через артерии. Иногда эти отложения могут внезапно отделиться и образовывать сгусток, который вызывает сердечный приступ или инсульт перемещаясь с кровотоком к сердцу или мозгу.
Откуда в нашей крови берутся липиды?
95% всех жиров, которые мы съедаем, составляют триглицериды (ТГ). Остальные 5 % приходится на фосфолипиды, свободные жирные кислоты, жирорастворимые витамины и холестерин. Липиды нужны клеткам нашего организма для выработки энергии – 1 гр. липидов генерирует 9 ккалорий, а 1 гр. белков или углеводов только 4 ккал. И еще для многих других целей, например для производства гормонов, синтеза клеточных оболочек, синтеза желчных кислот.
Липиды попадают в кровь из двух источников: из пищи и в процессе метаболизма в печени и жировой ткани. В крови они циркулируют не сами по себе, а с помощью переносчиков – липопротеинов. Нашему организму для нормальной работы нужны разные виды липидов.
Триглицериды – это особенная разновидность жиров, потребляемых нами вместе с пищей, которая расходуется на производство и поддержание энергии, или откладываются в жировой ткани. Триглицериды являются также основным сырьем для производства холестерина в печени.
Холестерин
Холестерин необходим для синтеза желчи, а желчь нужна нам для пищеварения. Холестерин используется также для синтеза некоторых гормонов и для строительства клеточных оболочек. Холестерин почти полностью производится в печени, но в небольшом количестве попадает к нам с пищей животного происхождения. В растительной пище холестерин не содержится.
Липопротеины
Липиды – это жирорастворимые органические вещества. Они не растворяются в воде, а, значит, и в крови. Для того, чтобы циркулировать в крови и достигать органов и клеток жиры должны связываться со специальными переносчиками – липопротеинами. Белковая оболочка липопротеинов надежно защищает заключенные в ней липиды, как ракушка хранит свою жемчужину, а также помогает липидам попадать в те клетки, где эти липиды нужны, открывая их, как ключ открывает замок.
Основными типами липопротеинов являются:
| ЛПОНП – липопротеины очень низкой плотности | ЛПНП – липопротеины низкой плотности | ЛПВП – липопротеины высокой плотности |
| Основные переносчики триглицеридов. Транспортируют триглицериды в места их хранения и использования. В небольшой своей части они также отвечают за транспортировку холестерина. | Основные переносчики холестерина к клеткам организма. ХС ЛПНП часто называют «плохим» холестерином, так как они способны откладываться на стенках артерий, что приводит к сужению их просвета и затруднению кровотока. | ЛПВП состоят в основном из протеиновых оболочек. Холестерин, содержащийся в них, обозначается как ХС ЛПВП и условно считается «хорошим» холестерином. Они помогают удалению избытка холестерина из кровотока. |
Наследственность или высокий холестерин по наследству
Высокий уровень холестерина часто может передаваться по наследству и диагностироваться только при сдаче лабораторных анализов по причине возникновения сердечного приступа или инсульта. Немедленно сообщите своему врачу, если у кого-то из членов вашей семьи были такие заболевания особенно в молодом возрасте и подумайте о сдаче анализов.
Семейная гиперхолестеринемия является наследственным заболеванием, которое вызывает атипично высокие уровни холестерина липопротеинов низкой плотности (ЛПНП-Х). При этом заболевании печень не в состоянии утилизировать естественный запас холестерина, который постоянно вырабатывается. В результате холестерин становится опасно переизбыточным, что резко увеличивает риск отложений атеросклеротических бляшек и развития у человека ишемической болезни сердца (недостатка кислорода, поступающего к сердцу из-за сужения сосудов). Представьте себе неисправную утилизацию мусора через мусоропровод. Каждую ночь вам нужно выбросить новый мусор и испорченную пищу, но предыдущие отходы уже забили трубы. Как вы уже догадались, это скоро приведет к катастрофе. Если ваша печень не фильтрует и не перерабатывает холестерин ЛПНП должным образом, это мало чем отличается от неправильной утилизации мусора. Сосуды наиболее страдают из-за отложений бляшек холестерина они сужаются и имеют меньшую эластичность.
Возможные причины снижения уровня холестерола
Жирный спирт или холестерол – еще одно название известного всем холестерина. Механизм снижения его концентрации в организме слабо изучен, но на основе имеющихся данных, можно сделать следующие выводы. Вероятными причинами возникновения патологии, специалисты называют:
- Тяжелые заболевания печени. Именно этот орган синтезирует до 80% общего количества холестерола, поэтому болезни печени приводят к падению его уровня.
- Иррациональная диета. Речь идет об игнорировании пищи, содержащей жиры и предпочтении продуктов с быстрыми углеводами.
- Авитаминозы. Дефицит необходимых организму веществ из-за голодания, тяжелых инфекционных болезней, анорексии.
- Длительное состояние стресса. Адреналин, вырабатывающийся при нервных перегрузках, являет антагонистом жирных спиртов.
- Патологии щитовидной железы. К примеру, гипертиреоз сопровождается тяжелым нарушением продукции и баланса основных гормонов. Изменения гормонального фона – еще одна причина снижения его концентрации в крови.
- Прием подавляющих синтез жирных спиртов препаратов. Привести к чрезмерному их снижению, способна неадекватная дозировка статинов, фибратов, никотиновой кислоты.
Кроме того, провоцирующими гипохолестеринемию признаны продолжительные лихорадочные состояния, вызванные инфекционными заболеваниями (туберкулез, пневмонии) или травмами. Неблагоприятными факторами возникновения, также становятся анемии или наследственные аномалии, часто связанные с нарушениями функции печени.
У женщин, изменения концентрации холестерина крови, нередко возникают при беременности. Особенно, если она осложнена рецидивом хронических заболеваний.
Симптомы высокого холестерина
Иногда холестерин откладывается и на поверхности кожных покров (в виде бляшек на коже лица, нижних веках, конечностях и туловище, но наиболее опасные отложения холестерина внутри нашего организма, которые не видны. Часто высокий уровень холестерина низкой плотности в организме не имеет симптомов. И в большинстве случаев заболевание остается вовремя не выявленным, что может привести к сердечному приступу, инфаркту миокарда, инсульту в раннем возрасте, а также проблемам с атеросклерозом.
Анализы на холестерин и липидный профиль
Липидный профиль измеряет:
- бщий холестерин;
- олестерин, связанный с ЛПВП(липопротеидами высокой плотности или альфа — липопротеидами), которые могут уменьшать или затормаживать увеличение “плохого” холестерина в крови);
- олестерин липопротеидов очень низкой плотности (пре-бета – липопротеиды которые являются главной транспортной формой триглицеридов. Их относят к высоко атерогенным липопротеидам, участвующим в механизме образования атеросклеротических бляшек;
- олестерин, переносимый частицами ЛПНП (липопротеидами низкой плотности, бета — липопротеидами) то есть плохой холестерин, который способствует заболеванию сосудов);
Вы можете сдать эти основные показатели в отдельности или заказать более обширный анализ липидного профиля по программе 112 липидный комплекс или 113 липидный комплекс расширенный которые включают дополнительно исследования
- Уровня триглицеридов;
- Индекс атерогенности;
- Наличие Аполипопротеина – А 1, Аполипопротеина– В;
- Ліпопротеина (а) — дополнительных факторов развития атеросклероза;
Как расшифровать анализ крови
Узнать, повышен ли общий холестерин можно, проведя анализ крови в лаборатории. Если общий холестерин повышен — что это значит, как действовать, и все о лечении объяснит врач. Но попробовать расшифровать результаты анализов можно и самостоятельно. Для этого нужно знать, что биохимический анализ вмещает три показателя: х-н ЛПНП, х-н ЛПВП и общий холестерин.
Липидограмма – это комплексное исследование, позволяющее оценить липидный обмен в организме, которое позволяет определить, как происходит липидный обмен и рассчитать риск проявления атеросклероза и ИБС.
Правильная расшифровка липидограммы крови важна и сточки зрения оценки необходимости приема статинов, суточная доза таких препаратов. Статины – препараты, имеющие много побочных эффектов, при этом цена их достаточно высокая. Поэтому, исходя из того, что это такое – липидограмма, этот анализ позволяет узнать, из чего состоит кровь человека, и назначить наиболее эффективную терапию пациенту.
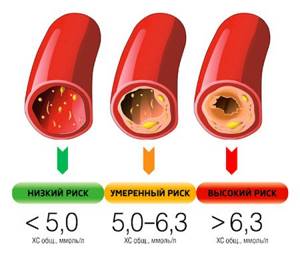
Уровень холестерина и развитие атеросклероза сосудов
Ведь общий холестерол – это показатель, который сам по себе не дает возможности четко оценить вероятность проявления у пациента атеросклероза. Если холестерол общий повышен, что делать, можно оценить по полному спектру диагностических показателей. Поэтому определяются следующие показатели:
- ЛПВП (альфа-холестерин) – определяется, липопротеиды высокой плотности повышены или понижены. Учитывается, при определении показателей в-липопротеидов, что это вещество выполняет защитную функцию, предотвращая развитие атеросклероза.
- ЛПНП – липопротеины низкой плотности повышены или понижены. Чем выше показатель бета-холестерина, тем больше активизируется атеросклеротический процесс.
- ЛПОНП – липопротеиды очень низкой плотности, благодаря ним транспортируются экзогенные липиды в плазме. Синтезируются печенью, являются главным предшественником ЛПНП. ЛПОНП принимают активное участие в продукции атеросклеротических бляшек.
- Триглицериды – это сложные эфиры высших жирных кислот и глицерина. Это транспортная форма жиров, следовательно, их повышенное содержание также повышает риск атеросклероза.
Какой должен быть холестерин в норме, определяется в зависимости от возраста, он может быть разным у женщин и мужчин. Кроме того, важно понимать, что точного числа, которым обозначается норма холестерина — нет. Существуют лишь рекомендации, каким должен быть индекс. Следовательно, если показатель отличается и отклоняется от диапазона, то это является свидетельством какой-либо болезни.
Однако тем, кто собирается сдать анализ, следует учесть, что при проведении анализа могут допускаться определенные погрешности. Данные проведенного исследования засвидетельствовали, что в 75% лабораторий страны такие погрешности допускаются. Что делать, если вы стремитесь получить точный результат? Лучше всего сделать такие анализы в тех лабораториях, которые сертифицированы ВЦС («Инвитро» и др.)
Норма холестерина у женщин
- в норме у женщин показатель общего холестерина: 3,6 — 5,2 ммоль/л;
- х-н, повышенный умеренно: 5,2 — 6,19 ммоль/л;
- х-н, повышенный значительно: более 6,19 ммоль/л.
- х-н ЛПНП: нормальный показатель – 3,5 ммоль/л, повышенный – от 4,0 ммоль/л.
- х-н ЛПВП: нормальный показатель – 0,9-1,9 ммоль/л, опасным для здоровья считается уровень ниже 0,78 ммоль/л.
| № | Возраст (лет) | Общий холестерин (ммоль/л) |
| 1 | младше 5 | в пределах 2,90-5,18 |
| 2 | 5-10 | в пределах 2,26-5,30 |
| 3 | 10-15 | в пределах 3,21-5,20 |
| 4 | 15-20 | в пределах 3,08-5,18 |
| 5 | 20-25 | в пределах 3,16-5,59 |
| 6 | 25-30 | в пределах 3,32-5,75 |
| 7 | 30-35 | в пределах 3,37-5,96 |
| 8 | 35-40 | в пределах 3,63-6,27 |
| 9 | 40-45 | в пределах 3,81-6,53 |
| 10 | 45-50 | в пределах 3,94-6,86 |
| 11 | 50-55 | в пределах 4,20-7,38 |
| 12 | 55-60 | в пределах 4,45-7,77 |
| 13 | 60-65 | в пределах 4,45-7,69 |
| 14 | 65-70 | в пределах 4,43-7,85 |
| 15 | от 70 | в пределах 4,48-7,25 |
Норма холестерина у мужчин
- в норме показатель общего холестерина у мужчин: 3,6 — 5,2 ммоль/л;
- х-н ЛПНП: нормальный показатель – 2,25 — 4,82 ммоль/л;
- х-н ЛПВП: нормальный показатель – 0,7 — 1,7 ммоль/л.
| № | Возраст (лет) | Общий холестерин (ммоль/л) |
| 1 | до 5 | в пределах 2,95-5,25 |
| 2 | 5-10 | в пределах 3,13-5,25 |
| 3 | 10-15 | в пределах 3,08-5,23 |
| 4 | 15-20 | в пределах 2,93-5,10 |
| 5 | 20-25 | в пределах 3,16-5,59 |
| 6 | 25-30 | в пределах 3,44-6,32 |
| 7 | 30-35 | в пределах 3,57-6,58 |
| 8 | 35-40 | в пределах 3,78-6,99 |
| 9 | 40-45 | в пределах 3,91-6,94 |
| 10 | 45-50 | в пределах 4,09-7,15 |
| 11 | 50-55 | в пределах 4,09-7,17 |
| 12 | 55-60 | в пределах 4,04-7,15 |
| 13 | 60-65 | в пределах 4,12-7,15 |
| 14 | 65-70 | в пределах 4,09-7,10 |
| 15 | от 70 | в пределах 3,73-6,86 |
Триглицериды
Триглицериды являются определенным типом жиров, которые содержатся в крови человека. Они – основной источник энергии и наиболее распространенный тип жиров в организме. Развернутый анализ крови определяет количество триглицеридов. Если оно в норме, то эти жиры являются полезными для организма.
Как правило, повышены триглицериды в крови у тех, кто потребляет большое количество килокалорий, чем сжигает. При повышенном их уровне часто отмечается так называемый метаболический синдром, при котором отмечается повышенное давление, увеличен сахар в крови, отмечается низкое содержание хорошего х-на, а также есть большое количество жира вокруг талии. Такое состояние повышает вероятность развития диабета, инсульта, болезней сердца.
Норма триглицеридов – 150 мг/дл. Норма триглицеридов у женщин в крови, как и у мужчин, превышена, если показатель больше 200 мг/дл. Однако показатель до 400 мг/дл. обозначается как допустимый. Высоким уровнем принято считать показатель 400-1000 мг/дл. очень высоким – от 1000 мг/дл.
Если триглицериды понижены, что это значит, нужно спрашивать у врача. Такое состояние отмечается при болезнях легких, гипертиреозе, инфаркте мозга, поражении паренхимы, миастении, при приеме витамина С и др.
Когда рекомендуют сдавать анализы на холестерин?
Молодые люди без факторов риска сердечно-сосудистых заболеваний обычно проходят тестирование один раз в возрасте от 17 до 19 лет. Повторное тестирование для взрослых без факторов риска для сердечных заболеваний обычно проводится каждые пять лет.
Американская кардиологическая ассоциация рекомендует проводить тестирование холестерина каждые 4 – 6 лет для людей в возрасте 20 лет и старше.
Пациенты принимающие лекарства при повышенном уровне холестерина, например статины, должны проверять уровень холестерина по рекомендации врача или через 4 – 12 недель после первой дозы, а затем каждые 3 –12 месяцев после этого. Рекомендуется исследовать уровень холестерина не реже одного раза в пять лет, если у человека общий холестерин составляет 5,2 ммоль или есть предпосылки для развития сердечно-сосудистых заболеваний и инсульта. Дополнительные причины возможного развития сердечных заболеваний включают сахарный диабет, высокое кровяное давление или использование антигипертензивных препаратов), низкий уровень ЛПВП, семейный анамнез ишемической болезни сердца (ИБС) и гиперхолестеринемию, а также курение сигарет.
Комплексы с этим исследованием
Фитнес-мониторинг Обследование для выбора физнагрузки и мониторинга состояния организма 4 970 Р Состав
Диетолог рекомендует Оценка состояния обмена веществ 5 640 Р Состав
Профилактический чек-ап Универсальный ежегодный профилактический скрининг 8 710 Р Состав
В ДРУГИХ КОМПЛЕКСАХ
- Мужская антивозрастная диагностика 10 140 Р
- Метаболический профиль 4 740 Р
- Антивозрастная диагностика в постменопаузе 9 620 Р
- Расширенная женская антивозрастная диагностика 22 900 Р
- Контроль рациона кормящей мамы 2 250 Р
Факторы риска наличия повышенного холестерина включают в себя:
- Несбалансированное питание, употребление насыщенного жира, содержащегося в продуктах животного происхождения, и транс-жиров, содержащихся в некотором печенье, соусах, крекерах и даже попкорне, красное мясо, жирные молочные продукты могут повысить уровень холестерина;
- Ожирение. Наличие индекса массы тела (ИМТ) 30 или выше повышает риск высокого уровня холестерина;
- Недостаток физических упражнений. Упражнения помогают повысить уровень ЛПВП или «хорошего» холестерина;
- Курение. Курение сигарет повреждает стенки кровеносных сосудов, делая их более склонными к накоплению жировых отложений. Курение также может снизить уровень ЛПВП или «хорошего» холестерина»;
- Пожилой возраст. Поскольку химические процессы меняются с возрастом, риск высокого уровня холестерина возрастает. Например, с годами печень становится менее способной удалять холестерин ЛПНП;
- Сахарный диабет. Высокий уровень сахара в крови способствует повышению уровня опасного холестерина, называемого липопротеидами очень низкой плотности (ЛПОНП), и снижению уровня холестерина ЛПВП. Высокий уровень сахара в крови также повреждает слизистую оболочку артерий что способствует отложению холестерина на поврежденных участках;
- Повышенное давление. Это является сигналом наличия проблем с сердечно-сосудистой системой которые возникают при высоком уровне холестерина;
- Заболевания печени и желудочно-кишечного тракта способствуют нарушению обмена холестерина;
- Эндокринные заболевания также влияют на синтез холестерина.
Осложнения высокого уровня холестерина
- Развитие атеросклероза. Высокий уровень холестерина может вызвать опасное накопление холестерина и других отложений на стенках артерий (атеросклероз). Эти отложения (бляшки) могут уменьшить кровоток через артерии;
- Стенокардия (ишемическая болезнь сердца). Если поражены артерии, которые снабжают сердце кровью (коронарные артерии), могут беспокоить появляющиеся боли в груди (стенокардия) или другие симптомы ишемической болезни сердца;
- Инфаркт. Если холестериновые бляшки на стенках сосудов разрываются в месте повреждения может образоваться сгусток крови (тромб). Сгусток блокирует поток крови, закупоривая сосуд ниже по течению. Если кровоток в части органа прекращается, возникает некроз его тканей (омертвение), что наблюдается, например, при инфаркте миокарда;
- Инсульт. Подобно сердечному приступу, инсульт возникает, когда сгусток крови блокирует кровоток в части мозга.
Нормальный уровень липидов в крови
В современном мире, в странах, где нет недостатка еды, для поддержания нормального уровня липидов в крови основным условием является ограничение калорийности ежедневного рациона и употребление с пищей «правильных» жиров. Искомый уровень холестерина в крови, который часто называется целевым уровнем, поддерживается нормальной работой печени, способной синтезировать недостающее количество любого из липидов. Если все эти процессы уравновешены – на стенках артерий не происходит вредных отложений.
Профилактика
Чтобы помочь предотвратить высокий уровень холестерина, вы можете:
- Регулярно обследоваться в лаборатории Дила;
- Соблюдать диету с низким содержанием соли и преобладанием фруктов, овощей, цельного зерна;
- Ограничить количество животных жиров и использовать растительные жиры в умеренных количествах;
- Поддерживать здоровый вес;
- Бросить курить и уменьшить потребление алкоголя;
- Делать физические упражнения не менее 30 минут в день;
- Контролировать уровень стресса, которому вы подвергаетесь;
Пониженный уровень холестерина
Пониженный — это так же проблема. Так как холестерин является важным компонентом клеточных мембран, предшественником гормонов, желчных кислот и других компонентов, имеющих важное значение в живом организме, уменьшение его количества имеет негативные последствия
- Выяснилось, что люди с низким уровнем холестерина чаще имеют симптомы депрессии и тревоги;
- Существуют исследования, которые доказывают возможную связь между низким уровнем холестерина и риском развития рака;
- Холестерин необходим для нормального синтеза половых гормонов, беременности и нормального менструального цикла. Низкий уровень холестерина может быть связан с риском преждевременных родов или рождения ребенка с низким весом;
Внешние симптомы гипохолестеринемии могут проявляться по-разному у каждого человека, но лабораторная диагностика помогает узнать их причину
Когда можно заподозрить сниженный уровень холестерина или гипохолестеринемию?
- При регулярном недоедании, строгих диетах;
- При наличии заболеваний со сниженной функций печени (в том числе циррозов, гепатитов);
- Воспалительных заболеваниях кишечника или энтеропатиях с потерей белка;
- При гипертиреозе или гипоадренокортицизме (болезни Аддисона). Пониженное количество глюкокортикоидов может снизить кишечную абсорбцию холестерина;
- Если вы подвергаетесь хроническому стрессу;
- При гипертиреозе или сверхактивной щитовидной железе;
- Надпочечниковой недостаточности;
- При мальабсорбции (недостаточном всасывании питательных веществ из кишечника), например, при целиакии;
- При лейкемии.
Вторичный гипогонадизм у мужчин
28.12.2020
4570
0
В продолжение первого доклада о первичном гипогонадизме у мужчин андролог, уролог, заведующий отделением андрологии и урологии НМИЦ акушерства, гинекологи и перинатологии имени В.И. Кулакова профессор Сафар Исраидович Гамидов выступил с обширной лекцией об особенностях вторичного гипогонадизма у мужчин и доступных режимах терапии.
С.И. Гамидов
Д.м.н., профессор, ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова» (г. Москва)
Как напомнил Сафар Исраилович, для специалиста-андролога обязательным является понимание физиологической роли гормонов, умение интерпретировать эндокринные показания с диагностической целью, а также назначать гормональные препараты с ожидаемым терапевтическим эффектом.
Существует ряд случаев, когда андрологу следует задуматься о назначении гормональной терапии:
- детская урология: крипторхизм, гипоспадия, микропенис;
- гипогонадизм, в том числе с ассоциированной эректильной дисфункцией;
- гиперпролактинемия;
- бесплодие (олигозооспермия, фрагментация ДНК сперматозоидов);
- необходимость в мужской контрацепции;
- приапизм;
- доброкачественная гиперплазия простаты;
- рак простаты с неблагоприятными прогностическими признаками.
Репродуктивная функция у мужчин работает благодаря гипоталамо-гипофизарно-гонадной системе. В гипоталамусе важно инфундибулярное ядро, содержащее KNDy-нейроны (субпопуляция нейронов аркуатного ядра) и ГнРГ-нейроны. В переднем гипофизе гонадотрофы вырабатывают лютеинизирующий (ЛГ) и фолликулостимулирующий (ФСГ) гормоны. В свою очередь, гонады продуцируют половые стероиды и гаметы под влиянием ЛГ и ФСГ.
В регуляции гипоталамо-гипофизарно-гонадной системы важную роль играют тестостерон, эстрадиол, ЛГ, ФСГ, пролактин, активины и ингибины, а также антимюллеров гормон.
В 1977 г. группы A. Schally и R. Guillemin были удостоены Нобелевской премии за открытие гонадолиберина (гонадотропин-релизинг-гормона, ГнРГ). Он представляет собой достаточно простой декапептид. Сначала носил название «ЛГРГ», но затем выяснилось, что он регулирует секрецию не только ЛГ, но и ФСГ. Как пояснил Сафар Исраилович, у человека присутствует в среднем лишь 1000–1500 ГнРГнейронов. Они вырабатывают ГнРГ, который попадает в систему воротных вен гипоталамо-гипофизарного аппарата. ГнРГ циркулирует в веночной сети гипоталамуса и гипофиза.
У женщин важную роль в регуляции менструального цикла играют пульссекреция и выбросы ГнРГ. У здоровых мужчин есть только один режим его секреции — пульс-секреция. За сутки происходит около 10–20 секреторных импульсов, и не существует пейсмейкеров, которые могли бы четко их регулировать. Секреция гонадотропинов (ЛГ и ФСГ) передней доли гипофиза стимулируется пульсирующим высвобождением ГнРГ и ингибируется высвобождением гонадотропин-ингибирующего гормона из гипоталамуса. ЛГ и ФСГ имеют общую a-субъединицу и отдельную ß-субъединицу. ЛГ стимулирует и повышает продукцию тестикулярного андрогена клетками Лейдига, а ФСГ стимулирует сперматогенез в клетках Сертоли [1–3].
ФСГ является полезным индикатором для оценки функционального состояния мужского герминогенного эпителия, хотя и далеким от совершенства. Несмотря на большой разброс нормативных показателей (1,4–18,1 МЕ/л), по мнению ряда авторов, значения данного гормона > 4,5 МЕ/л уже свидетельствуют о высоком риске нарушения сперматогенеза. Кроме того, нестимулированный ФСГ является плохим предиктором успешного хирургического лечения сперматозоидов у мужчин с необструктивной азооспермией (НОА) [4, 5].
В практике встречаются мутации рецепторов ФСГ и ЛГ. Мутации гена ФСГ-ß у мужчин неизменно приводят к азооспермии и уменьшению размеров яичек. По некоторым научным данным, имеющиеся мутации рецепторов ФСГ обеспечивают разной степени влияние на мужскую фертильность. При этом в зависимости от характера мутации выраженность изменений сперматогенеза может проявляться от тяжелой олигозооспермии до нормозооспермии с возможностью зачатия естественным способом. Эти клинические данные хорошо коррелируют с результатами экспериментальных работ, полученными на моделях мышей. Модели мышей с измененными ЛГ-рецепторами демонстрируют снижение уровня сывороточного и интратестикулярного тестостерона и возникновение позднего блока сперматогенеза [3, 6, 7].
Важным фактором в формировании фертильности является уровень тестостерона. В частности, большое проспективное когортное исследование 357 мужчин с идиопатическим бесплодием и 318 фертильных мужчин показало, что у бесплодных мужчин значительно снижены уровень общего и свободного тестостерона, соотношение тестостерон / ЛГ, а также тестостерон / эстрадиол (р < 0,001) [8].
К основным известным эндокринным регуляторам сперматогенеза относятся тестостерон (регулирует количество бледных сперматогоний, эффект на другие этапы сперматогенеза не доказан) и ФСГ (основной фактор, регулирующий все этапы сперматогенеза, кроме мейоза). С клинической точки зрения, синергизм тестостерона и ФСГ необходим для инициации и поддержания активного сперматогенеза [3].
Что касается андрогеновых рецепторов, иммуногистохимический анализ тканей яичка у бесплодных мужчин показал изолированное распространение андрогеновых рецепторов только на клетки Сертоли. Экспрессия этих рецепторов в клетках Сертоли и адекватные интратестикулярные концентрации тестостерона необходимы как для завершения мейоза половых клеток, так и для пролиферации сперматогоний. Повреждение андрогеновых рецепторов клеток Сертоли у мышей приводит к ранней остановке сперматогенеза. Недостаточная интратестикулярная концентрация тестостерона связана с нарушением целостности гематотестикулярного барьера у мышей. Увеличение дозы тестостерона и ФСГ способствует развитию in vitro герминальных клеток, полученных у мужчин с ранним и поздним блоком сперматогенеза, до сперматид, и это позволяет выполнить процедуру ISCI [9–12].
Исследования с аспирационной биопсией яичек у фертильных мужчин подтвердили, что тестостерон является преобладающим интратестикулярным андрогенным гормоном. Концентрация интратестикулярного тестостерона составляет 60 000 нг/дл, что намного выше, чем средняя концентрация сывороточного тестостерона у мужчин (500 нг/дл). В исследовании концентрация интратестикулярного тестостерона превышала концентрацию ГСПГ, что свидетельствует о том, что большая часть внутриклеточного тестостерона, вероятно, находится в биодоступной форме [13].
Используя новые методы анализа, те же авторы показали, что 70% всего интратестикулярного тестостерона составляет биологически активное вещество. При этом концентрация общего тестостерона сыворотки слабо коррелировала с концентрацией интратестикулярного тестостерона (р = 0,38). По данным новых тестов, сывороточные биоактивные андрогены также слабо коррелируют с интратестикулярным уровнем биологически активного андрогена (r = 0,46; p = 0,03).
Уровни сывороточного и интрастестикулярного тестостерона, измеренные одновременно, сильно коррелировали между собой в исследованиях (r = 0,67, p = 0,03). Кроме того, была обнаружена значительная вариабельность интратестикулярного уровня тестостерона, корая очень сильно коррелировала с сывороточным ЛГ (r = 0,87; p = 0,01). По мнению авторов, пульсирующая секреция ЛГ может отражать аналогично пульсирующую секрецию интратестикулярного тестостерона. Пульсирующая секреция интратестикулярного тестостерона была также подтверждена при оценке концентрации тестостерона и эстрадиола в канюлированных венах половых желез у мужчин с варикоцеле. Отбор проб каждые 15 мин выявил ежечасные импульсы тестостерона (3–5 импульсов в час) со средней амплитудой 176 +/– 42 нг/мл, что в 6,6 раза больше, чем надир. Вместе с тем сегодня влияние интратестикулярной пульсирующей секреции тестостерона на сперматогенез неизвестно [14]. Впрочем, та же экспериментальная работа показала, что сперматогенез в яичке сохраняется до тех пор, пока уровень интратестикулярного тестостерона не упадет ниже 75% от базовой концентрации. Однако четкий уровень интратестикулярного тестостерона, при котором сперматогенез человека нарушается, до конца не уточнен.
Многообещающим биомаркером интратестикулярного андрогенного статуса является инсулиноподобный белок — 3 (INSL3), который секретируется зрелыми клетками Лейдига. Аспирация яичек и анализ сыворотки крови подтвердили, что INSL3 тесно коррелирует с интратестикулярным тестостероном как во время индуцированного гипогонадизма, так и после лечения ХГЧ (r = 0,79, p < 0,001). При этом ингибин В и антимюллеров гормон не коррелировали с интратестикулярным тестостероном. Несмотря на эти многообещающие результаты, INSL3 еще не используется в рутинной клинической практике в качестве биомаркера функции клеток Лейдига и интратестикулярного андрогенного статуса [15].
Важным показателем степени сперматогенеза является ингибин В. В случае гипосперматогенеза его секреция снижается, а секреция ФСГ увеличивается. В одном проспективном исследовании было обнаружено, что ингибин В и ФСГ значительно коррелируют с основными показателями спермограммы. Вместе с тем значения коэффициента корреляции для ингибина В выше, чем для ФСГ (ингибин В: 0,48; р < 0,0001, ФСГ: 0,41; р = 0,0007) [16].
Противоположным действием обладает активин. Он является гетеродимером или гомодимером ß-субъединиц и также вырабатывается в семенниках. Активин оказывает агонистическое действие на секрецию ФСГ гипофизом, и его высвобождение ингилируется ингибином В. Активин в настоящее время не используют в клинической оценке мужской фертильности [17].
В 2001 г. был обнаружен пептид кисспептин. Он оказывает агонистическое действие на высвобождение ГнРГ и пульсирующее высвобождение ЛГ. Кисспептин был использован экспериментально у мужчин для индуцирования секреции гонадотропинов. Экспериментально показано, что введение кисспептина сопровождается более выраженным увеличением ЛГ, чем ФСГ. В настоящее время кисспептин не используется в клинической практике [18].
Эстрадиол вырабатывается из тестостерона с помощью ароматазы, входящей в семейство цитохромов Р450. Концентрация эстрадиола у мужчин в крови низкая, но чрезвычайно высокая в сперме, а его содержание в яичке может достигать 250 пг/мл, что выше, чем в сыворотке крови у женщин. По имеющимся научным данным, только использование тестостерона и эстрадиола приводит к снижению уровня ЛГ и ФСГ в сыворотке крови. Ингибирующий эффект эстрадиола на ЛГ оказывается за счет снижения чувствительности к ГнРГ. Дигидротестостерон, который не превращается в эстрадиол, не оказывал ингибирующий эффект на секрецию гонадотропинов [19, 20].
Для нормального сперматогенеза необходим достаточный уровень эстрадиола в яичке, что доказано клиническими исследованиями с участием бесплодных мужчин с врожденным дефицитом ароматазы. Рецепторы к эстрадиолу экспрессируются в клетках Сертоли и Лейдига, как и в герминальных клетках. Экспериментальные животные с поврежденным рецептором к эстрадиолу бесплодны и имеют аномальный сперматогенез. Эстроген снижает регуляцию связанных со сперматогенезом генов и индуцирует апоптоз сперматоцитов через эстрогеновые рецепторы 1 и 2. Эстроген регулирует реабсорбцию просветной жидкости в головке придатка яичка. По имеющимся данным, бесплодие у данной категории животных происходит за счет нарушения реабсорбции жидкости из проксимального отдела эпидидимиса и последующего повышения внутрипросветного давления. Данное открытие вызывает обеспокоенность по поводу потенциального прямого воздействия андрогенов окружающей среды на репродукцию самцов и сообщений по поводу снижения количества сперматозоидов у человека [21–23].
Также участвуют в репродукции ароматазы ферменты цитохрома Р450, который необратимо преобразует андрогены в эстрогены в различных тканях, включая яичко, печень, мозг и жировую клетчатку [21, 24]. В яичке ароматаза локализована в клетках Лейдига [25]. В большом ретроспективном когортном исследовании была обнаружена связь между бесплодием, основными параметрами спермы и сниженным соотношениям тестостерон/эстрадиол. Это соотношение < 10 было расценено как точка отсечения 20-го процентиля среди фертильных мужчин. В частности, подобное снижение соотношения тестостерон/эстрадиол наблюдается у тучных мужчин из-за повышенной периферической ароматизации [26].
Также клетки Сертоли экспрессируют рецепторы тиреоидиных гормонов. Помимо этого, тиреоидные гормоны влияют на развитие клеток Лейдига и стероидогенез. Таким образом, гормоны щитовидной железы могут поддерживать различные популяции половых клеток. Отмечается связь между тератозооспермией и наличием клинической картины гипер- или гипотиреоза [27, 28].
В физиологических условиях при резком повышении концентрации пролактина в крови может усилиться секреция тестостерона. Многие исследователи полагают, что связанный со сном пик секреции тестостерона у мужчин частично обусловлен увеличением содержания пролактина в плазме крови. При хронической гиперпролактинемии у мужчин ингибируются импульсные выбросы ГнРГ, и, следовательно, секреция гонадотропинов и уровень тестостерона в крови снижаются [29].
Как напомнил Сафар Исраилович, в организме присутствует несколько видов регуляции. Аутокринная регуляция — наличие рецепторов к ГнРГ, каннабиоидам и опиоидам в гипоталамусе. Паракринная регуляция — наличие рецепторов к ГнРГII и ЛГ, которые ретроградно поступают в гипоталамус посредством портального кровотока. Эндокринная регуляция — тестостерон и эстрадиол замыкают цепь отрицательной обратной связи на гипофизе и гипоталамусе соответственно.
К регуляторам активности ГнРГ-нейронов в целом относятся эстрадиол, прогестерон, дигидротестостерон, тестостерон, эстрадиол, кортизол, пролактин, гамма-аминомасляная кислота, активины и ингибины, эндоканнабиноиды, опиоиды, серотонин, лептин и мелатонин.
Гипогонадотропный гипогонадизм связан с дефицитом продукции ГнРГ и ЛГ/ФСГ. Бывает врожденным (с аносмией или без аносмии) и приобретенным (черепно-мозговые травмы, нейроинфекции, опухоли, операции). Очень редко встречается изолированный дефицит ЛГ (синдром Паскалини), казуистически редко — изолированный дефицит ФСГ [30].
Внутричерепные опухоли являются наиболее частой причиной приобретенных форм гипогонадотропного гипогонадизма. В отличие от приобретенных форм, этиология врожденного гипогонадотропного гипогонадизма более сложна и большинстве случаев носит идиопатический характер. Распространенность врожденного гипогонадотропного гипогонадизма у мужчин составляет 1/10000 [31].
До 90% случаев вторичного гипогонадизма не сопровождается признаками органического поражения яичек или других компонентов гипоталамо-гипофизарногонадной оси. Для этих ситуаций предложен термин «функциональный гипогонадизм» [32, 33]. До 85% мужчин с сексуальной дисфункцией при низком уровне тестостерона имеют признаки метаболического синдрома.
Перечень лекарственных препаратов, применяемых при гипогонадизме, достаточно широк:
- ингибиторы обратного захвата серотонина;
- антиаритмические препараты (амиодарон);
- антиконвульсанты (фенитоин);
- противогрибковые препараты (кетоконазол);
- опиаты;
- антипсихотики;
- статины в высоких дозах;
- тиазидные диуретики;
- спиронолактон;
- циметидин.
Для дифференциальной диагностики гипогонадотропного гипогонадизма от конституциональной формы задержки полового созревания необходимо учитывать результаты следующих тестов:
- физический осмотр;
- анализ кариотипа;
- определение уровня половых гормонов;
- тест с аналогом ГнРГ;
- определение костного возраста;
- МРТ гипоталамо-гипофизарной области.
Выделяется ряд главных целей и задач терапии гипогонадотропного гипогонадизма. Так, цели гормональной терапии в этом случае — поддержание функции яичек, развитие вторичных половых признаков, улучшение качества жизни и восстановление репродуктивной функции. Ключ к успеху лечения гипогонадотропного гипогонадизма — это выбор адекватного препарата с соответствующей дозой. Препараты тестостерона, гонадотропинов и ГнРГ с пульсирующей помпой могут использоваться в гормональной регуляции пациентов с гипогонадотропным гипогонадизмом. При необходимости сохранения репродуктивной функции у данной категории больных наиболее предпочтительны гонадотропины [34].
При терапии гипогонадотропного гипогонадизма ХГЧ 1000–1500 ед. 3 раза в неделю или по 2500 ед. 2 раза в неделю в течение 3–6 месяцев основными целями являются нормализация уровня тестостерона, переход темных А-клеток в бледные А-клетки и пролиферация пула герминальных клеток. При терапии ФСГ по 75– 150 ед. 3 раза в неделю (рекомбинантный, очищенный или в составе менопаузального гонадотропина) зона инъекции не должна совпадать с ХГЧ. ФСГ стимулирует превращение бледных А-клеток в В-клетки и последующий мейоз, инициирует сперматогенез [35].
Сперматогенез обычно восстанавливается за 6–9 месяцев, хотя у некоторых пациентов процесс может затянуться до двух лет. Примерно у 10% больных, несмотря на терапию с использованием ХГЧ и ФСГ, сперматогенез не восстанавливается вовсе [36]. Эффективность терапии не зависит от этиологии гипогонадотропного гипогонадизма: прогнозировать результат позволяет только объем яичек [37]. Пороговое значение объема яичек для прогнозирования эффективности терапии гонадотропинами — 4 см3 [38].
В частности, в исследовании 36 мужчин от 11 до 42 лет с гипогонадотропным гипогонадизмом (у 81% — первичный и у 19% — вторичный) практиковалась длительная терапия препаратами хорионического гонадотропина — от 12 до 240 месяцев (в среднем 56). Увеличение количества сперматозоидов среди больных с уменьшенными размерами яичек отмечено в 36% случаев, а при нормальных размерах яичек увеличение концентрации сперматозоидов отметили у 71% больных.
Некоторые авторы сегодня ошибочно считают, что ХГЧ является аналогом ЛГ. Это не так. В частности, олигосахаридные цепочки защищают ХГЧ от биодеградации. Также возможно развитие иммуноопосредованной резистентности к ХГЧ [39]. В целом, комбинированная терапия с применением ХГЧ и ФСГ позволяет добиться больших успехов, чем монотерапия. Среди побочных эффектов такого лечения отмечались акне и гинекомастия.
Согласно одному из доступных исследований десятилетнего опыта использования ХГЧ и МГЧ по отдельности и вместе для лечения больных гипогонадотропным гипогонадизмом, на фоне комбинированной терапии, по сравнению с ХГЧ, достоверно чаще отмечалось увеличение объема яичек (75 против 50% соответственно). У 86% пациентов, получавших комбинированное лечение, в конечном итоге удалось добиться сперматогенеза, по сравнению с 81% среди тех, кто получал только ХГЧ [40]. Примерно в 10% случаев гипогонадотропный гипогонадизм спонтанно разрешается после прекращения комбинированного лечения. Факторы риска неудачи лечения включают крипторхизм и маленький объем яичек (менее 4 мл).
Альтернативным способом стимуляции сперматогенеза у данной категории больных может являться инфузия ГнРГ в пульсирующем режиме. Хоффман и Кроули в 1982 г. использовали гонадорелин в качестве подкожной инфузии в импульсном режиме у пациентов с гипогонадотропным гипогонадизмом и добились у них индукции сперматогенеза [41, 42]. Также китайские исследователи в 2010 и 2011 гг. сообщили об успешном использовании импульсной подкожной инфузии ГнРГ для запуска сперматогенеза при гипогонадотропном гипогонадизме, однако размер выборки этих исследований был относительно небольшим [43, 44].
Пульс-терапия аналогами ГнРГ требует установки подкожной или венной помпы и имитирует естественную пульс-секрецию ГнРГ, при этом требуется регулярная смена канюли каждые 2–3 дня. Этот метод считается оправданным только при гипогонадотропном гипогонадизме с азооспермией. По сравнению с терапией ХГЧ+ФСГ, такой метод требует меньше времени для восстановления сперматогенеза, при нем наблюдается меньше пиков тестостерона, меньше частота развития акне и боли в грудных железах, однако выше частота местных кожных реакций [43].
В 2021 г. было предпринято рандомизированное контролируемое исследование CONSORT для сравнительной оценки эффективности гормональной терапии гипогонадотропного гипогонадизма в разных режимах с участием 220 пациентов. Участники были разделены на четыре группы. Группа 1 — ГнРГ при врожденном гипогонадотропном гипогонадизме, группа 2 — ГнРГ при приобретенном гипогонадотропном гипогонадизме, группа 3 — ХГЧ/МГЧ при врожденном гипогонадотропном гипогонадизме и группа 4 — ХГЧ/МГЧ при приобретенном гипогонадотропном гипогонадизме. Оценка эффективности производилась через 18 месяцев [45]. Группа ГнРГ получала подкожные инфузии гонадорелина в дозе от 100 до 500 мг в день с помощью специальной помпы — каждые 90 мин (16 импульсов за 24 ч). В зависимости от уровня ФСГ, ЛГ и тестостерона производилась корректировка дозы препарата. Симультанно были использованы раствор ХГЧ в дозе 5000 МЕ и МГЧ в дозе 75 МЕ. Доза МГЧ составила от 75 до 150 МЕ во внутримышечных инъекциях один или два раза в неделю. Доза ХГЧ — от 5000 до 10 000 МЕ внутримышечно один или два раза в неделю. Дозу препаратов корректировали в зависимости от уровня тестостерона и продуктивности сперматогенеза, причем уровень тестостерона поддерживался на отметке 10–15 нмоль/л. Авторы показали, что любой подход к терапии является эффективным: через 25 месяцев после начала терапии у 90% пациентов достигалось хотя бы минимальное присутствие сперматозоидов в эякуляте, однако концентрация сперматозоидов 10–15 млн/мл достигалась только у 50% мужчин. У пациентов, которые достигали более высоких пиковых уровней ЛГ на фоне терапии, частота получения сперматозоидов в эякуляте была выше.
В некоторых случаях больным могут назначаться селективные модуляторы рецепторов к эстрогенам (SERM), при этом частой ошибкой является бессмысленный прием таких препаратов, в частности кломифена. При истинном гипогонадотропном гипогонадизме отсутствует субстрат для активности SERM. В случае вторичного гипофизарного гипогонадизма отсутствуют гонадотрофы гипофиза, и нет клеток, способных синтезировать ЛГ и ФСГ. Гипоталамический гипогонадизм — «третичный», при нем нет смысла устранять отрицательную обратную связь, если нет положительного стимулирующего фактора (ГнРГ). Наконец, при гипогонадизме, ассоциированном с гиперпролактинемией, выработка ГнРГ не нормализуется, если не устранить избыточный уровень пролактина. При повышенном уровне пролактина, в частности, использование каберголина способно значительно улучшить гормональные показатели пациентов и помочь в восстановлении сексуальной функции [46].
В заключение Сафар Исраилович напомнил, что гипоталамо-гипофизарно-гонадная ось — это хрупкая структура, в функционирование которой лучше не вмешиваться без оснований и четкого понимания своих действий. Лучший способ лечения гипогонадизма у мужчин, не заинтересованных в сохранении фертильности, — тестостерон-заместительная терапия. Монотерапия ХГЧ в большинстве случаев, за некоторыми исключениями, неоправданна и сопряжена с рисками. Следует помнить, что для нормального сперматогенеза необзодимы и тестостерон, и ФСГ. Наконец, при гипогонадизме и эректильной дисфункции имеет смысл провести исследование на пролактин сыворотки крови.
Источники:
- Ubuka T et al. Front Endocrinol, 2014
- Kumasi TR. Cell Endocrinol, 2007
- Layman LC et al. J Clin Endocrinol, 2002
- Kwee J et al. Fertil Steril, 2008
- Ramasamy R et al. J Urol, 2013
- Kumar TR. Molec Cell Endocrinol, 2007
- Siegel ET et al. Reprod Sci, 2013
- Andersson AM et al. J Clin Endocrinol Metab, 2004
- Tesarik J et al. Fertil Steril, 2002
- Kato Y et al. Andrology, 2014
- De Gendt K et al. A Proc Nat Acad Sci USA, 2004
- Cheng CY et al. Prarmacol Rev, 2012
- Jarow JP et al. Ann NY Acad Sci, 2005
- Roth MY et al. J Androl, 2010
- Roth MY et al. Fertil Steril, 2013
- Meachem SJ et al. Eur J Endocrinol, 2001
- Hedger, MP et al. Mol Cell Endocrinol, 2012
- Skorupskaite K. Hum Reprod Upd, 2014
- Bagatell C et al. J Androl, 1994
- Hayes FJ et al. Clin Endocrinol Metab, 2000
- Carreau S et al. Adv Med Sci, 2012
- Hess RA et al. Nature, 1997
- Eddy EM et al., 1996
- Schlegel PN. Fertil Steril, 2012
- Inkster SJ. J Clin Endocrinol Metab, 1995
- Saylam B et al. Fertil Steril, 2011
- Mintziori G. Endocrinol Invest, 2016
- Kumar A. Indian J Endocrinol Metab, 2014
- Corsello SM et al. Clin Endocrinol, 2003
- Mao JF et al. Asian J Androl, 2017
- Varimo T et al. Hum Reprod, 2017
- Grossman, Matsumoto, 2017
- Corona, Maggi, 2015
- Lin et al. Medicine, 2019
- Arroyo et al., 2015
- Schiff et al., 2007
- Farhat et al., 2010
- Miyagawa Y, Tsujimura A. J Urol, 2005
- Leao, Esteves, 2014
- Yang L. Int Urol Nephrol, 2012
- Belchetz PE et al. Science, 1978
- Dwyer AA. Best Pract Rec Clin Endocrinol Metab, 2015
- Zhang GY. Reprod and Contracept, 2010
- Sun Y et al. Clin J Endocrinol Metab, 2011
- Lin et al. Medicine, 2019
- De Rosa M et al. J Clin Endocrinol Metab, 2004
Материал подготовила Шадеркина В.А. Видео можно посмотреть на Uro.TV
Комментарии
Для отправки комментариев необходимо войти или зарегистрироваться