Комплексы с этим исследованием
Планирование беременности. Клинические показатели 6 630 Р Состав
Причины выпадения волос 2 500 Р Состав
Биохимия крови. 19 показателей Расширенный биохимический анализ крови 6 280 Р Состав
В ДРУГИХ КОМПЛЕКСАХ
- Обследование во время беременности. 3 триместр 9 620 Р
- Мужской чек-ап №1 18 570 Р
- Женский чек-ап №1 19 290 Р
- Биохимия крови. 8 показателей 990 Р
- Обследование во время беременности. 1 триместр 16 690 Р
Подробное описание исследования
Сывороточное железо — это микроэлемент, который не вырабатывается в организме человека самостоятельно, а поступает только извне с пищей.
Железо входит в состав:
- Гемоглобина, который является главным переносчиком кислорода легких к тканям и органам;
- Миоглобина, который находится в мышцах и отвечает за создание кислородного резерва.
Также железо участвует в клеточном обмене, в работе иммунной системы, входит в состав некоторых ферментов, обеспечивая нормальное протекание в них метаболических реакций, а также участвует в синтезе ДНК.
Всего в организме находится не более 5г железа. Оно поступает с пищей из животных и растительных источников. Это так называемое гемовое (содержится в мясных продуктах, в составе гемоглобина) и негемовое (ферменты и белки растительной пищи) железо. Из общего количества железа, которое поступило в организм, всасывается всего около 10%. Процесс всасывания происходит в двенадцатиперстной кишке.
В плазме крови человека большая часть железа находится в окисленном трехвалентном состоянии в связке с белком трансферрином. Трансферрин переносит железо к тканям и органам. Большая часть поступающего железа уходит на образование гемоглобина, а оставшаяся часть депонируется (запасается). Основное депо железа в организме — это специальные белковые комплексы «ферритин» и «гемосидерин». Отсюда железо расходуется в случае его снижения в сыворотке крови. Восстановление железа сыворотки крови зависит от степени наполнения депо. При длительной нехватке железа его запасы истощаются, что может привести к анемии. Данный механизм регуляции обеспечивает самосохранение.
Концентрация сывороточного железа — важный биохимический показатель, изменение которого может указывать на возможные проблемы обмена этого микроэлемента.
Дефицит железа встречается чаще, чем его переизбыток. Как правило, человек не замечает, что у него развивается анемия — патологическое снижение концентрации гемоглобина крови. Обычно это становится заметно, когда концентрация гемоглобина становится ниже 100 г/л. Тогда человек может жаловаться на повышенную утомляемость, головокружение, выпадение волос, бледность кожи и ломкость ногтей. В некоторых случаях люди отмечают ощущение покалывания и жжения кончика языка.
Если не предпринимать никаких действий, направленных на восстановление депо железа, дальше развивается одышка, рассеянность внимания, учащенное сердцебиение (тахикардия).
Подобные состояния наблюдаются при онкологических заболеваниях (особенно если поражен кишечник), железодефицитных анемиях, желтухе, острых и хронических инфекциях, язвенной болезни и язвенном колите. Дефицит железа часто может быть вызван хронической кровопотерей при геморрое. При целиакии, болезни Крона и в послеоперационном периоде также диагностируют анемию. Концентрация железа у женщин изменяется в зависимости от фазы менструального цикла.
Также встречается так называемая «анемия беременных» — состояние при котором снижается концентрация сывороточного железа у беременных женщин. Как правило, во втором триместре, когда формируется депо железа у плода. Это состояние также требует особого наблюдения.
Переизбыток железа встречается реже и характеризуется следующими симптомами: боли в животе и суставах, нарушение сердечного ритма, а также, схожая с анемией, усталость.
Для нормальной работы всех органов и систем необходимо, чтобы с пищей в день поступало не менее 1 мг железа. Продукты питания богатые этим микроэлементом: мясо и субпродукты (свиная печень), бобовые (чечевица, фасоль), зелень (шпинат, сельдерей), фрукты (гранат, яблоки). Аскорбиновая кислота улучшает процесс всасывания железа, поэтому рекомендуется употреблять ее вместе с железосодержащими продуктами. Помешать усвоению железа могут молочные продукты и кофеин.
Показания к исследованию
На ранних стадиях недостатка микроэлемента клинические проявления, как правило, отсутствуют. По мере усугубления ситуации появляются следующие жалобы на здоровье:
- одышка;
- слабость, постоянное чувство усталости;
- бледность кожи;
- болевые ощущения в области груди;
- приступы головокружения;
- частые головные боли.
Иногда при недостатке микроэлемента наблюдаются такие характерные симптомы, как ощущение жжения на языке, появление нестандартных пищевых пристрастий (например, возникает желание есть глину), язвочки небольшого размера в уголках рта. Часто анализ крови на железо назначается после выявления отклонений в результатах ОАК, который проводится во время профилактического обследования или по другим причинам.
Использованная литература
- Федеральные клинические рекомендации по диагностике и лечению железодефицитной анемии, 2015. — 58 с.
- Клочкова-Абельянц, С.А., Суржикова, Г.С. Железодефицитная анемия и анемия хронических заболеваний: некоторые аспекты патогенеза и перспективы дифференциальной диагностики. — Медицина в Кузбассе, 2021. — №3. — С.25-28.
- Tiglis, M., Neagu, T., Niculae, A. et al. Incidence of Iron Deficiency and the Role of Intravenous Iron Use in Perioperative Period, 2021. — Vol. 56(10). — P. 528.
Железодефицит у беременных
Железодефицитная анемия — одно из тех редких осложнений беременности, которое можно легко предотвратить на этапе планирования. Даже здоровые беременные подвержены риску развития анемии в связи с физиологической гемодилюцией и расходованием запасов железа для роста плода и материнского эритропоэза [1]. Учитывая тот факт, что развивающийся плод очень требователен к концентрации кислорода и железа в поступающей к нему крови, плацента способна увеличивать количество рецепторов к железу и хранить его в резидентных ретикулоэндотелиальных клетках [1,3]. Следует различать дефицит железа и железодефицитную анемию (ЖДА). Распределение железа в организме идет преимущественно в пользу гемового железа, следовательно, развитие анемии на фоне железодефицита — это сигнал о выраженном недостатке микроэлемента в депо [3]. В связи с этим выделяют три стадии дефицита: предлатентный — снижение резервного железа без уменьшения расходования его на эритропоэз, латентный — истощение депо и дефицит транспортного железа, без признаков анемии и манифестный или ЖДА [8].
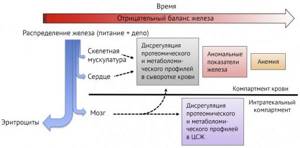
Рисунок 1 | Изменения в организме на различных стадиях железодефицита. Синей стрелкой указано распределение поступающего в организм железа — в первую очередь на эритропоэз, затем на синтез миоглобина и ферментные системы. Красной стрелкой указано прогрессирование дефицита с течением времени [3].
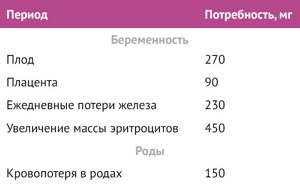
Потребность в железе на разных сроках беременности варьирует. В первом триместре суточная потребность снижается по сравнению с небеременным состоянием преимущественно за счет отсутствия менструальной кровопотери, а также за счет снижения эритропоэза. Во втором триместре объем циркулирующей крови увеличивается на 45 %, объем плазмы — на 50 %, а масса эритроцитов — на 35 %, следовательно, потребность в железе растет. В третьем триместре максимально возрастает потребность плода в железе, а кровопотеря в процессе родов уносит с собой около 150 мг железа [4].
Таблица 1 | Среднее увеличение потребности в железе в период беременности и в послеродовом периоде для женщин с массой тела до беременности от 55 до 60 кг [4,9]
Факторы риска развития железодефицита и железодефицитной анемии у женщин детородного возраста [4,8]:
- нарушения диеты (вегетарианство или веганство, недостаточное употребление красного мяса, анорексия, булимия, чрезмерное употребление кальция, чая, кофе);
- нарушения всасывания питательных веществ (болезнь Крона, целиакия);
- паразитозы (анкилостомоз, лямблиоз, цестодоз, шистосомоз);
- хронические заболевания (малярия, ВИЧ, гемоглобинопатии, аутоиммунные заболевания, ЗНО);
- осложнения беременности (рвота беременных, преэклампсия, холестатический гепатоз);
- короткие интервалы между беременностями (менее года);
- меноррагия;
- донорство крови.
Проявления дефицита крайне неспецифичны и могут списываться женщиной на саму беременность: быстрая утомляемость, слабость, раздражительность, нарушение концентрации внимания, бледность кожи и слизистых, головная боль, головокружение, тахикардия, одышка, усталость в ногах. Некоторые женщины отмечают пристрастие к специфическим продуктам: сырому мясу, сырым крупам, мелу, почве [1,8,10].
Существуют определенные опасности, связанные с дефицитом железа: повышение риска послеродовой депрессии, послеродового кровотечения (предположительно из-за снижения сократительной способности матки в условиях дефицита кислорода в тканях), некоторые исследования также говорят о риске развития послеродового сепсиса [1,10]. Женщин с анемией чаще подвергают гемотрансфузиям и родоразрешают путем кесарева сечения [2]. Преимущественно в странах с низким уровнем доходов показатели гемоглобина < 70 г/л связаны с двукратным увеличением материнской смертности [1,10]. В послеродовом периоде анемия связана с повышенной утомляемостью, депрессивными расстройствами, снижением познавательных способностей, нарушением лактации и ранним прекращением грудного вскармливания [10].
Железо в организме плода делится на гемовое железо, негемовое железо и депо, находящееся преимущественно в печени. В эритроцитах содержится 55 мг/кг железа в виде гемоглобина, нормальная концентрация которого у доношенных детей составляет 133–184 г/л. В депо хранится около 12 мг/кг железа в виде ферритина, нормальная концентрация которого в пуповинной крови доношенного ребенка составляет 170 мг/л. Наименьшее количество железа (около 8 мг/кг) участвует в метаболических процессах и переносе кислорода в мышцах. Дефицит негемового железа трудно отследить из-за отсутствия специфических биомаркеров, лабораторно он обнаруживается только в совокупности с дефицитом железа в депо и, как следствие, сниженным ферритином. Концентрация ферритина < 76 мг/л связана с нарушением неврологических функций новорожденного [3]. В случае легкой и умеренной степени дефицита у матери, компенсаторные механизмы поддерживают адекватное поступление железа плоду, но тяжелый дефицит, приводящий к развитию ЖДА у матери, приводит к развитию железодефицита у ребенка [5].
Регуляция биодоступности железа во время беременности, частично зависит от концентрации гепсидина у матери. Гепсидин — гормон-регулятор, вырабатывающийся в печени и регулирующий концентрацию железа в плазме и распределение его в тканях. Гепсидин действует путем ингибирования поступления железа в кровь, влияя на абсорбцию в кишечнике, высвобождение железа из макрофагов и мобилизацию его из депо. Гормон действует через рецептор ферропортин (Fpn), экспрессирующийся во всех тканях экспортирующих железо в плазму. Связывание гепсидина и ферропортина запускает секвестрацию железа в клетках-мишенях и снижение его поступления в плазму, следовательно, существует обратная зависимость между концентрацией гепсидина и достаточным потреблением железа тканями, в том числе костным мозгом и плацентой [9].
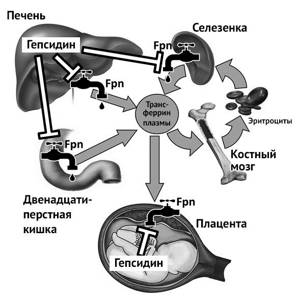
Рисунок 2 | Регуляция гомеостаза железа в организме беременной женщины. Fpn — ферропортин, Fe-Tf — трансферрин
В отношении влияния на развитие плода и исходы для новорожденного все не так однозначно: считается, что анемия матери связана с более высоким риском перинатальной и неонатальной смертности, низкой массой тела при рождении, преждевременными родами, однако метаанализ рандомизированных клинических исследований по влиянию добавок железа на перинатальные исходы показал лишь умеренное влияние на массу тела при рождении и неопределенное влияние на частоту преждевременных родов [1,2]. В то же время, некоторые исследования сообщают о 30% увеличении риска развития задержки роста плода на каждые 10 г/л сниженного гемоглобина до 20 недель беременности, а снижение гемоглобина <100 г/л значительно увеличивало риск мертворождения и перинатальной смерти. [10]. Постнатальный дефицит железа течение первых девяти месяцев в значительной степени обусловлен уровнем железа при рождении, следовательно, существует прямая зависимость между железодефицитом матери и плода. Самые распространенные факторы развития анемии у плода: острое материнское или плацентарное кровотечение и тяжелый дефицит железа у плода (менее 90 г/л). К другим факторам, приводящим к железодефициту плода, относятся артериальная гипертензия у матери, курение, нарушенная толерантность к глюкозе / сахарный диабет при нормальных показателях гемоглобина и ферритина, а также многоплодная беременность [3].
Наибольший интерес представляет влияние дефицита железа на нейрокогнитивные функции ребенка. Недостаток железа у матери в третьем триместре приводит к структурным изменениям головного мозга новорожденного, включая изменения в сером веществе: нейроны имеют более простую структуру, нарушается функционирование митохондрий. Железосодержащие ферменты играют важную роль в синтезе жирных кислот, являющихся неотъемлемой частью миелина, в связи с чем, дефицит железа в раннем возрасте изменяет жировой состав миелина и приводит к гипо- и дисмиелинизации нервной системы. Железодефицит изменяет экспрессию генов, критических для развития и функционирования гиппокампа, а также изменяет концентрацию нейротрансмиттеров, зависящих от железосодержащих гидроксилаз – тирозингидроксилазы и триптофангидроксилазы (дофамин, серотонин, норэпинефрин), нарушает работу их рецепторов и механизмов обратного захвата, что неминуемо приводит к ряду психоневрологических расстройств. [3,10].
У новорожденных с неанемическим дефицитом железа и концентрацией ферритина пуповинной сыворотки < 40 мг/л отмечаются нарушения памяти распознавания (способности узнавать ранее встречающихся людей, события, объекты), как и у двухмесячных младенцев с концентрацией ферритина пуповинной сыворотки < 76 мг/л. Нарушения памяти распознавания отмечались также в возрасте до 3,5–4 лет у детей с низким неонатальным уровнем железа, даже если в постнатальном периоде дефицита не было. Учитывая тот факт, что железодефицитная анемия у матери является предрасполагающим фактором для развития железодефицита у младенцев, создаются предпосылки для нарушения психомоторного развития ребенка. Дефицит железа в младенчестве и детстве связан с более низкой скоростью обработки информации, нарушением неврологических рефлексов, ухудшением двигательной функции, трудностями с социализацией, что в свою очередь создает предпосылки для развития тревожных и депрессивных расстройств в будущем. У детей в возрасте 5–6 лет отмечаются трудности с обучением, планированием и концентрацией внимания [3,10].
Существуют определенные риски, связанные с развитием психических расстройств у детей, рожденных от матерей с железодефицитной анемией. Низкий уровень железа в преконцепционном периоде связывают с высоким риском развития аутизма, во втором триместре — с повышением риска развития шизофрении на 30 % [3].
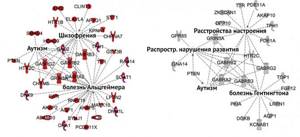
Рисунок 3 | Изменения экспрессии генов при железодефиците. Слева – непосредственное влияние дефицита на экспрессию, справа – эпигенетические нарушения. [3]
Как правило, железодефицит наряду с другими анемиями диагностируется во время рутинного исследования уровня гемоглобина в рамках общего анализа крови. Диагностика анемии у беременных имеет некоторые особенности в связи с вариабельностью показателей гемоглобина в зависимости от триместра. Для первого триместра пороговым значением является Hb < 110 г/л, для второго – < 105 г/л, в послеродовом периоде – < 100 г/л. В развернутом анализе крови рассчитываются эритроцитарные индексы: МНС (среднее количество гемоглобина в эритроците), MCV (средний объем эритроцита), МСНС (средняя концентрация гемоглобина в эритроците). Для дефицита характерно снижение показателей, однако, следует помнить о физиологическом увеличении MCV в время беременности [1,6].
Для железа существуют специфические маркеры: ферритин, различные методы оценки насыщения трансферрина: трансферрин, уровень растворимых рецепторов трансферрина (sTSAT), %TSAT (коэффициент насыщения трансферрина) и гепсидин – пептидный гормон, реагирующий на избыток железа. Концентрация гемоглобина в ретикулоцитах также определяет преанемию, дефицит железа и, следовательно, может служить ранним биомаркером дефицита железа [3,5]. Сывороточное железо и общая железосвязывающая способность сыворотки в настоящее время считаются ненадежными маркерами в связи с влиянием употребления железа и суточными колебаниями значений [6].
Таблица 2 | Диагностические критерии железодефицитной анемии у беременных. ПДЖ – предлатентный дефицит железа, ЛДЖ – латентный дефицит железа, МДЖ – манифестный дефицит железа. [7,8]
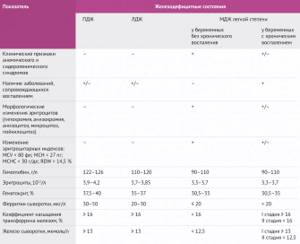
Наиболее широко у беременных используется ферритин – маркер депонирования железа в печени матери и плаценте. Именно ферритин поддерживает стабильный уровень железа, выводя из депо необходимое для синтеза гема количество. Диагностически значимым является снижение уровня сывороточного ферритина <30 мкг/л. Но в случае с сопутствующим системным воспалением ферритин может сыграть злую диагностическую шутку: уровень маркера растет, маскируя железодефицит, в связи с чем рекомендуется параллельное исследование С-реактивного белка для проведения дифференциальной диагностики [1,3,6].
Трансферрин — белок, отвечающий за транспорт железа в плазме крови, реагирующий на его дефицит увеличением концентрации. Показатель sTfR пропорционален количеству трансферрина. При снижении концентрации сывороточного железа концентрация sTfR возрастает одновременно с трансферрином. %TSAT рассчитывается путем деления уровня сывороточного железа на общую железосвязывающую способность сыворотки и умножения на 100. Он отражает процент участков связывания железа на трансферрине, которые заняты молекулами железа. Концентрация железа в сыворотке снижается на ранних этапах дефицита, тем самым снижая %TSAT. По мере усугубления дефицита концентрация трансферрина увеличивается, чтобы оптимизировать способность связывать железо для транспорта, что еще больше снижает %TSAT. Все эти изменения происходят до микроцитоза или анемии [3].
Самый интересный из предлагаемых маркеров — гепсидин, измерение концентраций которого в сыворотке может дать наибольшее количество информации о том, кто должен получать добавки железа, а кому они не показаны. Гепсидин — это главный регулятор всасывания железа в кишечнике и распределения железа из ретикулоэндотелиальных клеток, он синтезируется печенью в ответ на уровень железа и наличие воспаления. Гепсидин является негативным регулятором: это означает, что высокие его концентрации снижают всасывание железа в кишечнике и способствуют секвестрации железа, тогда как низкие уровни увеличивают абсорбцию железа в кишечнике и высвобождение железа ретикулоэндотелиальными клетками. Пациентки с низким уровнем гепсидина, вероятно, будут нуждаться в добавках железа и ответят на терапию, тогда как пациентки с высоким уровнем гепсидина из-за недостаточности железа или перегрузки им не нуждаются в дополнительном железе и не будут столь активно усваивать железо из пищи. Начало беременности характеризуется очень низкими концентрациями гепсидина, что указывает на состояние отрицательного баланса железа и дает веские доказательства того, что потребности в железе во время беременности высоки. Таким образом, женщины, уровень железа которых до беременности нормален или находится на границе нормы, склонны к развитию дефицита железа во время беременности [3].
Источники:
- Pavord S. et al. UK guidelines on the management of iron deficiency in pregnancy //Br J Haematol. – 2021.
- Stanley L Schrier, Michael Auerbach. Treatment of iron deficiency anemia in adults//UpToDate, Feb. – 2021.
- Georgieff M. K. Iron deficiency in pregnancy //American journal of obstetrics and gynecology. – 2021.
- McMahon L. P. Iron deficiency in pregnancy //Obstetric Medicine. – 2010.
- McCann S., Perapoch Amadó M., Moore S. E. The Role of Iron in Brain Development: A Systematic Review //Nutrients. – 2021.
- Клинические рекомендации “Кровесберегающие технологии в акушерской практике” 2014.
- Федеральные клинические рекомендации “Диагностика, профилактика и лечение железодефицитных состояний у беременных и родильниц” 2013.
- Доброхотова Ю. Э., Бахарева И. В. Железодефицитная анемия беременных: профилактика и лечение //РМЖ. – 2021.
- Fisher A. L., Nemeth E. Iron homeostasis during pregnancy //The American journal of clinical nutrition. – 2021.
- Benson C. S. et al. Iron deficiency anaemia in pregnancy: A contemporary review //Obstetric Medicine. – 2021.