Бак посев из уретры у мужчин — микробиологическое исследование состава микрофлоры уретрального канала. В норме у мужчин в уретре может находиться небольшое количество грамположительных кокков и палочек, а семявыводящие канальцы и простата должны быть стерильными.
Результаты данного исследования необходимы для диагностики инфекционных заболеваний мочеполовой системы и для выявления возбудителя инфекционного воспаления, а также для определения уровня фертильности.
У здоровых представителей мужского пола дистальные отделы уретры контаминируют с кокками и грамположительными палочками в небольших объемах. Проксимальные отделы уретры, семявыводящие пути и простата – стерильны.
Выделяемые возбудители (условно-патогенные бактерии): неферментирующие грамотрицательные бактерии, энтеробактерии, стрептококки, коринеформные бактерии, энтерококки, стафилококки, гемофилы и дрожжеподобные грибы.
Основа радикального и эффективного лечения — применение препаратов антибиотического ряда, определяемых за счет новейшего метода исследования – микробиологической диагностики.
Общая характеристика
Отделяемое из уретры исследуют с целью диагностики воспалительного процесса при уретритах различной этиологии (бактериальных уретритах, гонореи, трихомониазе, хламидиозе и др.). При исследовании отделяемого из уретры число и состав клеточных элементов зависят от остроты и продолжительности воспалительного процесса.Воспалительное состояние слизистой оболочки мочеиспускательного канала (уретры) выражается наличием более 4 полинуклеарных нейтрофилов в поле зрения. О глубине патологического процесса в уретре свидетельствует преобладание в препаратах цилиндрического и парабазального эпителия.
Негонококковые уретриты у мужчин: этиология и обоснование этиотропной терапии
Термин «негонококковые уретриты» (НГУ) впервые был предложен в 1954 г. для обозначения случаев воспаления уретрального канала, вызванного иной, чем гонококк, инфекцией. До этого происхождение всякого уретрита считали гонококковым, а случаи отсутствия в материале из уретры гонококка объясняли диагностическими трудностями.
Статистические данные свидетельствуют о том, что НГУ является широко распространенным заболеванием, как в Российской Федерации, так и за рубежом. Если в 1996 г. в США частота выявления НГУ составила 2 млн случаев за год (S. O. Aral и соавт., 1999), то к 2000 г. она уже выросла до 3 млн случаев за год (CDC, 2000). В мире, по суммарной оценке, регистрируют около 50 млн случаев НГУ в год (S. O. Aral и соавт., 1999). Только по официальным данным, НГУ в России ежегодно заболевают около 350 тыс. человек, однако эти цифры явно занижены из-за недостаточной регистрации инфекций, вызывающих НГУ.
Этиологические факторы НГУ
Негонококковые уретриты у мужчин могут быть вызваны самыми разнообразными возбудителями, включая облигатные патогены, такие как Chlamydia (C.) trachomatis или Mycoplasma (M.) genitalium, и условно-патогенные микроорганизмы, например другие микоплазмы, в частности Ureaplasma (U.) urealyticum. Причиной НГУ могут быть также вирусы и простейшие.
Роль хламидий в возникновении НГУ. В 70–80-е гг. прошлого века считалось, что около 50% и более случаев НГУ вызваны хламидийной инфекцией. Исследования последующих десятилетий продемонстрировали существенное снижение частоты уретритов у мужчин, вызванных C. trachomatis, — до 20% и менее (M. Shahmanesh, 2001; М. А. Гомберг и соавт., 2002; C. S. Bradshaw и соавт., 2006). В то же время в течение последних лет в Российской Федерации заболеваемость урогенитальной хламидийной инфекцией вышла на первое место среди всех бактериальных инфекций, передаваемых половым путем (ИППП). В нашей стране, начиная с 2004 г., это вторая по распространенности регистрируемая ИППП после трихомониаза.
Уретриты, вызванные С. trachomatis, проявляются обычно скудной клинической симптоматикой, но могут сопровождаться, хотя это нетипично, и признаками острого воспаления, сходными с теми, которые характерны для гонореи.
Роль генитальных микоплазм в возникновении НГУ. Установлено, что человек является естественным хозяином 13 видов микоплазм, из которых возможными возбудителями НГУ могут являться M. hominis, M. genitalium и U. urealyticum. Кроме этих видов микоплазм в урогенитальном тракте также обнаруживают M. fermentans, M. primatum, M. pirum, M. spermatophilum, M. penetrans, M. pneumoniae. Их роль и взаимодействие с организмом человека сегодня активно исследуются, но пока их значение в возникновении уретритов у мужчин не вполне ясно. Так, S. Sharma и соавторы (1998), используя полимеразную цепную реакцию (ПЦР) в дополнение к бактериологическому исследованию, выявили M. pneumoniae у мужчин, которые болели рецидивирующим уретритом и предъявляли жалобы на боль в области уретры и предстательной железы.
Вопрос о роли генитальных микоплазм в этиологии НГУ остается нерешенным из-за широкого распространения этих микроорганизмов и их частого выявления у лиц, не имеющих клинической симптоматики. Мнения исследователей по данному вопросу расходятся. Одни авторы склонны относить микоплазмы к облигатным патогенам, вызывающим уретриты, цервициты, простатиты, послеродовые эндометриты, пиелонефриты, бесплодие, различную патологию беременности и плода. Соответственно, по мнению этих авторов, следует добиваться эрадикации микоплазм в случае их выявления. Другие считают, что микоплазмы являются условно-патогенной флорой урогенитального тракта, и лишь при определенных условиях способны вызывать инфекционно-воспалительные заболевания мочеполовых органов. Большинство зарубежных авторов относят все микоплазмы, за исключением M. genitalium, к условно-патогенной флоре. Именно поэтому в МКБ-10 таких заболеваний, как «микоплазмоз», «уреаплазмоз» или «уреаплазменная инфекция», не зарегистрировано. По мнению многих исследователей, из микоплазм без всяких оговорок к числу патогенов, способных вызывать уретриты, можно отнести только M. genitalium. Однако опыты на экспериментальных моделях, эксперименты по аутоинокуляции культуры U. urealyticum, а также изучение иммунного ответа макроорганизма доказывают участие этих прокариотов в возникновении НГУ. Статистические исследования установили достоверную корреляцию между наличием в мазках из уретры уреаплазмы и хроническими НГУ, в то же время не выявлено достоверной взаимосвязи U. urealyticum c острыми НГУ (P. Horner, 2001). Также не доказана роль U. parvum в возникновении уретритов.
Показатели инфицированности урогенитального тракта микоплазмами весьма разноречивы и среди сексуально активного населения варьируют от 10 до 50%. У больных с НГУ U. urealyticum выделяют в 20–34% и выше (В. И. Кисина, 2002). Уреаплазмы, как правило, обнаруживают у людей, ведущих активную половую жизнь, а наиболее часто эти микроорганизмы выявляют у лиц, имеющих трех и более половых партнеров. Обобщенные данные об эпидемиологии M. genitalium были представлены David Taylor-Robinson (2001) на основе анализа работ 19 наиболее авторитетных исследователей, согласно которым эти микроорганизмы выделяли в 10–50% среди больных НГУ и у 0–17,7% здоровых лиц. Позже N. Dupin и соавторами (2003) было показано, что исчезновение этих микроорганизмов из уретры сопровождается разрешением уретрита, и наоборот — рецидив заболевания может быть связан с использованием препаратов, недостаточно активных в отношении M. genitalium.
Клиническая картина уретрита, при котором обнаруживаются микоплазмы, так же как при инфицировании хламидиями, не имеет патогномоничных симптомов. M. genitalium чаще обнаруживают у лиц с хроническими уретритами, вероятной причиной рецидивирования которых она является. L. Mena и соавторы (2002) показали, что пациенты с M. Genitalium-ассоциированными уретритами в меньшей степени, чем больные с гонококковыми уретритами, предъявляют жалобы на дизурию и выделения, а выделения у них гораздо реже носят гнойный характер.
Как и в большинстве случаев выявления условно-патогенной флоры, для микоплазм выделяют ряд факторов, способствующих развитию инфекционно-воспалительных процессов. Наиболее важными из них являются иммунные нарушения, изменения гормонального статуса, массивность колонизации, ассоциации с другими бактериями. Все эти факторы следует учитывать при выборе тактики ведения таких больных.
Роль аэробной и анаэробной сапрофитной флоры в возникновении НГУ. Роль различной сапрофитной флоры при НГУ весьма спорна. С одной стороны, очевидно, что часто высокие уровни колонизации этими бактериями урогенитального тракта обнаруживаются у мужчин с уретритом, но, с другой стороны, нередко такие же высокие показатели колонизации выявляются у мужчин без признаков воспаления. Можно предположить, что в ряде случаев отдельные представители условно-патогенной флоры или их ассоциации благодаря определенным условиям способны стать возбудителями уретрита, а в иных ситуациях они могут поддерживать воспаление, инициированное другими факторами.
Исследования пациентов с НГУ показали, что это заболевание может быть проявлением мочевой инфекции верхних отделов мочевыводящих путей, основную роль в которой играют грамотрицательные микробные агенты — Pseudomonas aeruginosa, Proteus spp., Escherichia coli и др.
(I. Schugt и соавт., 2004). Имеются также сведения об определенном значении грамположительной флоры — Staphilococcus spp., Corinebacterium spp. В таких случаях, когда роль этой флоры в возникновении НГУ вероятна, при выборе адекватной терапии необходимо определять чувствительность этих микроорганизмов к антимикробным препаратам (W. W. Li и соавт., 2003). Исследования, проведенные в начале 90-х гг. прошлого века (J. C. Lefevre и соавт., 1991), указывают на частое выявление у пациентов с уретритами Haemophilus spp., Gardnerella vaginalis, стрептококков группы В и Escherichia coli.
Возбудители кишечных инфекций привлекают к себе внимание как агенты, способные вызвать НГУ, в связи с возможностью передачи этих микроорганизмов при орогенитальных и аногенитальных контактах. На потенциальную способность энтеробактерий вызывать инфицирование уретры указывали Ю. К. Скрипкин и соавторы (1999). Как показал в своей работе В. П. Ковалык (2006), нередко НГУ, вызванные условно-патогенной флорой, являются следствием незащищенных орогенитальных и аногенитальных контактов.
При уретритах выявляются различные виды негонококковых нейссерий, причем в 85% случаев это Neisseria (N.) meningitidis (М. Maini и соавт., 1992). Вероятными путями передачи инфекции в этих случаях моут быть орогенитальный или аногенитальный половые контакты, которые имеются в анамнезе у большинства из этих пациентов. Изредка такие уретриты клинически сильно напоминают гонококковую инфекцию, сопровождаясь гнойными выделениями и значительно выраженной дизурией.
Часто при исследовании уретрального содержимого как у здоровых людей, так и у мужчин с НГУ выявляются анаэробные бактерии. Сведения о роли анаэробов в возникновении уретритов противоречивы. Большинство исследователей не нашли каких-либо свидетельств патогенной роли этих микроорганизмов. В ходе микробиологических исследований, посвященных сравнительному изучению бактериальной флоры уретры у здоровых и больных НГУ, существенных различий в этом вопросе выявлено не было. E. A. Fontaine и соавторы (1986) отмечали лишь, что Bacteroides urealyticus, возможно, причастны к небольшому количеству случаев НГУ вследствие того, что этот вид несколько чаще выявляют у мужчин с НГУ, чем у здоровых лиц.
О роли анаэробов косвенно можно было бы судить по результатам двойных слепых плацебоконтролируемых исследований по применению метронидазола, который активен в отношении этих микроорганизмов. Однако работы P. D. Woolley и соавторов (1990) показали, что применение метронидазола в дополнение к тетрациклину не позволило улучшить эффективность терапии НГУ. В то же время D. A. Hawkins и соавторы (1988), применяя метронидазол, обнаружили, что в тех случаях, когда заболевание было ассоциировано с анаэробными бактериями, положительная динамика отмечалась значительно чаще, чем в группе без анаэробов.
Кроме перечисленных представителей условно-патогенной флоры, этиологическим или ассоциированным агентом при НГУ, согласно данным литературы, оказывались Streptococcus (Str.) pneumoniae, Str. viridans, Str. mitis, Str. sanguis, Str. аnginosus, Str. agalactiae, Enterococcus faecium, N. subflava, N. perflava и N. flava, Staphilococcus (S.) aureus, S. epidermidis, Corynebacterium pseudodiphtheriae, бактерии, входящие в роды Enterobacter (Spp.), Proteus (Spp.), Branhamella (Spp.), Moraxella (Spp.), Pseudomonas (Spp.) и др.
Роль простейших в возникновении НГУ. Практически единственным представителем этой группы микроорганизмов, который может являться возбудителем уретрита, являются Trichomonas (T.) vaginalis. Они впервые были описаны Alfred Donne в 1837 г., задолго до открытия других ныне известных ИППП. Длительное время T. vaginalis рассматривали как урогенитальный патоген, вызывающий воспалительные заболевания женской половой сферы. В настоящее время доля этих простейших в этиологическом спектре НГУ у мужчин составляет, по некоторым сообщениям, до 17%. В то же время при обследовании мужчин, сексуальных партнеров инфицированных T. vaginalis женщин, трихомонады выделяли лишь в 14–60% случаев (J. N. Krieger и соавт., 1995). Трихомонадная инфекция у мужчин часто протекает бессимптомно. В случае наличия симптомов клиническая картина трихомонадной инфекции у мужчин представлена в большинстве случаев острым НГУ, как правило, коротким по продолжительности. Также простейшие выявляли у 15% больных персистирующим уретритом. Трихомонадная инфекция — одна из самых распространенных ИППП в мире: ежегодно ею заболевают около 174 млн человек (ВОЗ, 2001).
Существуют данные об этиологической роли при уретритах других простейших — Giardia lamblia и Entameoba histolytica (V. M. Licea и соавт., 2005; J. G. Meingassner и соавт., 1981), в основном у мужчин, имеющих секс с мужчинами.
Роль вирусов в возникновении НГУ. По современным представлениям, вирус простого герпеса (ВПГ) может быть причиной возникновения уретритов (P. J. Horner, 2001). Работы, проведенные с использованием современных методов диагностики, показали, что герпетические уретриты выявляются в 42,4–46,6% случаев у мужчин, страдающих рецидивирующим генитальным герпесом (Э. С. Балуянц, 1991; Т. Б. Семенова и соавт., 2001). По данным зарубежных исследований, частота обнаружения ВПГ при уретритах колеблется от 6 до 25% (P. D. Sturm и соавт., 2004; A. A. Oni и соавт., 1997). По данным В. П. Ковалыка (2006), у 44,4% больных с НГУ, возникшими после незащищенных орогенитальных контактов, этиологической причиной уретрита является ВПГ.
В. Н. Гребенюком и соавторами (1986) отмечено, что ассоциация ВПГ с грамотрицательными бактериями усиливает патогенность каждого возбудителя и является причиной устойчивости уретритов к лечению.
По данным N. Avgustinaki и соавторов (2004), у большинства пациентов с НГУ, ассоциированными с ВПГ первого и второго типа, в анамнезе нет указаний на эрозивные поражения половых органов, характерных для генитального герпеса.
Многие эксперты рекомендуют проводить исследования на ВПГ в качестве стандартного обследования при наличии синдрома выделений из уретры.
Аденовирусы также выделяли из урогенитального тракта у мужчин. Уретриты, ассоциированные с аденовирусами, чаще всего сопровождаются появлением эрозивно-язвенных поражений гениталий, конъюнктивитом, симптомами «простуды». Кроме того, клинические особенности уретрита включают наличие меатита и симптомов дизурии (C. S. Bradshaw и соавт., 2002). Первые сообщения появились в 1985 г. — при проведении иммунофлуоресцентного исследования авторы находили аденовирусы у 11,47% пациентов (S. Anghelescu и соавт., 1985). Эпидемиологические исследования последних лет указывают на то, что выделение аденовирусов происходит чаще в осенне-зимний период и встречается у 0,33–4% пациентов, обследующихся на ИППП (P. D. Swenson и соавт., 1995; C. S. Bradshaw и соавт., 2006).
В анамнезе у всех больных имелись незащищенные орогенитальные контакты.
Лечение больных с НГУ
Для разработки индивидуального плана лечения важно учитывать такие факторы, как вид возбудителя, давность инфицирования, история предшествовавшего лечения, наличия сопутствующей патогенной и условно-патогенной флоры.
Этиотропное лечение НГУ основывается на применении антибактериальных препаратов различных групп, активных в отношении основных возбудителей НГУ — хламидий и микоплазм. Активность препаратов в отношении любой инфекции определяется минимальной подавляющей концентрацией (МПК) в исследованиях in vitro. Показатели МПК, как правило, коррелируют с результатами клинического излечения. Оптимальными препаратами считаются антибиотики с наименьшей МПК, но следует помнить о важности таких параметров, как биодоступность, способность к созданию высоких внутритканевых и внутриклеточных концентраций, переносимость и комплаентность лечения.
Для выбора схемы адекватной терапии в конкретных случаях рекомендуется лабораторное определение чувствительности выделенных культур к различным антибиотикам. Но это в основном касается выявленной сапрофитной флоры. Так, многие авторы отмечают способность микоплазм быстро приобретать устойчивость к антибактериальным препаратам при их пассировании in vitro. Следовательно, необходимо тестирование свежевыделенных от больных штаммов. Другая сложность состоит в том, что при выявлении хламидий и микоплазм чувствительность к антибиотикам in vitro необязательно коррелирует с положительным эффектом in vivo. Это может быть связано с фармакокинетикой препаратов. Все эти факторы необходимо учитывать при назначении этиотропной терапии, которая во многих случаях может являться частью комбинированной терапии, особенно при смешанных инфекциях.
Европейское руководство по ведению больных с уретритами (2001) содержит рекомендации, согласно которым следует проводить лечение НГУ по базовым и альтернативным схемам.
Базовые схемы:
- доксициклин — 100 мг 2 раза в день в течение 7 дней;
- азитромицин — 1,0 г внутрь, однократно.
Альтернативные схемы:
- эритромицин — 500 мг 4 раза в день в течение 7 дней или 500 мг 2 раза в день в течение 14 дней;
- офлоксацин — 200 мг 2 раза в день или по 400 мг 1 раз в день, в течение 7 дней;
- тетрациклин — 500 мг 4 раза в день в течение 7 дней.
Из приведенных схем видно, что основными антибиотиками, рекомендованными для лечения НГУ, являются препараты тетрациклинового ряда, макролиды и фторхинолоны.
Специально разработанных официальных отечественных руководств по лечению НГУ пока нет, но существуют рекомендации по лечению отдельных разновидностей НГУ — трихомонадной, хламидийной и микоплазменных инфекций. Если обобщить рекомендации, изложенные в основных отечественных руководствах («Федеральное руководство по использованию лекарственных средств», «Рациональная фармакотерапия заболеваний кожи и инфекций, передаваемых половым путем» (под ред. акад. РАМН, профессора А. А. Кубановой), «Методические материалы по диагностике и лечению наиболее распространенных инфекций, передаваемых половым путем, и заболеваний кожи (протоколы ведения больных), изданных ЦНИКВИ), то можно представить следующие схемы этиотропного лечения НГУ.
Антибиотики тетрациклинового ряда. Основные препараты:
- доксициклин — по 100 мг 2 раза в сутки не менее 7–14 дней. Первая доза при приеме препарата составляет 200 мг.
Альтернативные препараты:
- тетрациклин — по 500 мг 4 раза в сутки в течение 7–14 дней;
- метациклин — по 300 мг 4 раза в сутки в течение 7–14 дней.
Макролиды. Основные препараты:
- азитромицин — однократный прием 1,0 г или по 250 мг 1 раз в сутки в течение 6 дней. Препарат принимают за 1 ч до еды или через 2 ч после еды;
- джозамицин — по 500 мг 2 раза в сутки в течение 7–14 дней.
Альтернативные препараты:
- эритромицин — по 500 мг 4 раза в день в течение 7–14 дней;
- рокситромицин — по 150 мг 2 раза в сутки в течение 7–14 дней;
- кларитромицин — по 250 мг 2 раза в сутки в течение 7–14 дней;
- мидекамицин — по 400 мг 3 раза в сутки в течение 7–14 дней.
Фторхинолоны:
- офлоксацин — по 200–300 мг 2 раза в день в течение 7–14 дней;
- спарфлоксацин — по 200 мг 1 раз в сутки в течение 10 дней (в первый день дозу удваивают);
- левофлоксацин — по 500 мг 1 раз в сутки в течение 10 дней;
- пефлоксацин — по 600 мг 1 раз в сутки в течение 7–14 дней.
Препараты тетрациклинового ряда являются самыми распространенными лекарственными средствами для этиотропного лечения больных НГУ. Несмотря на то что доксициклин применяется в лечении различной патологии несколько десятилетий, его активность против главных возбудителей НГУ остается высокой (D. Kilic и соавт., 2004).
Именно поэтому, согласно всем упоминавшимся выше рекомендациям, препаратом выбора при лечении НГУ является доксициклин. Преимуществом использования доксициклина является достаточно высокая эффективность и относительно небольшая стоимость лечения. Доксициклин по сравнению с тетрациклином имеет более высокую биодоступность, более длительный период полувыведения и лучше переносится. Кроме того, при использовании доксициклина, в отличие от других тетрациклинов, нет необходимости соблюдать диету, разработанную с учетом возможности связывания тетрациклинов с ионами Са2+. Наиболее частыми побочными эффектами при приеме препаратов тетрациклинового ряда являются тошнота, рвота, диарея, аллергические реакции. Эти реакции значительно менее выражены при использовании доксициклина моногидрата, а не традиционного доксициклина гидрохлорида. Доксициклина моногидрат (юнидокс солютаб) выпускается в уникальной лекарственной форме таблеток, которые могут приниматься внутрь целиком, могут быть разделены на части или разжеваны, могут быть растворены в воде с образованием сиропа-суспензии (при растворении в 20 мл воды) или раствора-суспензии (при растворении в 100 мл воды). Биодоступность доксициклина моногидрата (юнидокс солютаб) в указанной форме составляет 95%, что практически соответствует внутривенной инфузии.
В период лечения препаратами группы тетрациклинов больным необходимо избегать инсоляции из-за возможности фотосенсибилизации.
Этого побочного действия совершенно лишены антибиотики из группы макролидов. Все упомянутые руководства к препаратам выбора при лечении НГУ относят макролидный антибиотик азитромицин. Этому способствуют уникальные фармакокинетические характеристики азитромицина: продолжительный период полувыведения, высокий уровень всасывания и устойчивость к кислой среде, способность этого антибиотика транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, а также возможность проникновения внутрь клетки. Благодаря тому, что высокая терапевтическая концентрация азитромицина в тканях достигается после однократного приема стандартной дозы антибиотика и сохраняется в местах воспаления не менее 7 сут, с появлением азитромицина впервые возникла возможность эффективного лечения больных хламидийной инфекцией однократным приемом антибиотика внутрь. Сейчас на рынке появилось много дженериков азитромицина (например: азитрокс, хемомицин, зитролид). Оригинальным и наиболее известным препаратом азитромицина является сумамед, который используется в Российской Федерации с начала 90-х гг. прошлого века.
Преимуществами всех современных макролидных антибиотиков перед первым антибиотиком из этой группы эритромицином являются более высокая эффективность, улучшенная фармакокинетика, хорошая переносимость и меньшая кратность приема.
При приеме макролидов могут наблюдаться побочные эффекты со стороны желудочно-кишечного тракта (тошнота, рвота, диарея) и печени (повышение активности трансаминаз, холестаз, желтуха), а также аллергические реакции.
Наиболее благоприятный, по сравнению с другими макролидами, профиль безопасности имеет джозамицин. Частота побочных эффектов при его приеме не превышает 2–4%. Препарат не обладает гепатотоксичностью и почти не изменяет нормальную микрофлору кишечника. Кроме того, этот препарат в Российской Федерации разрешен к применению у беременных. На нашем фармацевтическом рынке джозамицин пока представлен единственным препаратом вильпрафен.
Необходимо обратить внимание, что уреаплазмы устойчивы к линкозаминам, но чувствительны к макролидам и стрептограминам, а остальные микоплазмы могут быть устойчивы к «старым» макролидам (эритромицин, ровамицин, олеандомицин) и стрептограминам, но высоко чувствительны к новейшим макролидам (джозамицин, кларитромицин) и линкозаминам.
Следующую группу препаратов, обладающих высокой активностью против широкого спектра возбудителей НГУ, составляют фторхинолоны. Единственными препаратами этой группы, которые авторы современных руководств рекомендуют для лечения хламидийной инфекции, являются офлоксацин и его усовершенствованный аналог — левофлоксацин. Ограничения в использовании фторхинолонов для лечения хламидийной инфекции связаны с тем, что в сравнении с антибиотиками других вышеперечисленных групп после терапии слишком высок процент рецидивов.
Такие фторхинолоны, как офлоксацин и спарфлоксацин, особенно высокоэффективны при НГУ, вызванных условно-патогенной сапрофитной флорой, так как обычно эта флора чувствительна к этим антибактериальным препаратам. Их «лидирующее положение» обусловлено широтой антибактериального спектра, высокой бактерицидной активностью, отличными фармакокинетическими характеристиками (быстротой всасывания, высокими концентрациями препарата в тканях, клетках, биологических жидкостях), низкой токсичностью. При лечении спарфлоксацином достигается более высокая комплаентность, так как препарат принимают лишь 1 раз в сутки. По данным Ю. Н. Перламутрова и соавторов (2002), спарфлоксацин также высокоэффективен при микоплазменной и уреаплазменной инфекциях.
Как и тетрациклины, фторхинолоны обладают фотосенсибилизирующим эффектом. Кроме того, препараты из группы фторхинолонов противопоказаны больным с нарушением функции печени и почек. Из побочных реакций после приема фторхинолонов могут наблюдаться диспепсические расстройства, тошнота, рвота, головокружение, аллергические реакции, тендиниты.
Для лечения трихомонадных НГУ рекомендован метронидазол — 2 г перорально однократно по 2,0 г в течение 3 дней или по 500 мг 2–3 раза в сутки в течение 5–7 дней. Кроме метронидазола, могут применяться и другие нитроимидазолы:
- орнидазол 1,5 г однократно по 500 мг 2 раза в сутки в течение 5 дней (при осложненных формах до 10 дней);
- тинидазол 2,0 г однократно в течение 3 дней или по 500 мг 2 раза в сутки в течение 5 дней;
- ниморазол 2,0 г однократно;
- секнидазол 2,0 г однократно или по 250 мг 2 раза в сутки в течение 10 дней.
Эти препараты обладают несколько лучшими фармакокинетическими параметрами, чем метронидазол, что позволяет снижать дозировки и кратность применения. При этом существенных преимуществ перед метронидазолом эти препараты не имеют, поскольку если трихомонады оказываются устойчивыми к метронидазолу, они будут устойчивы и к другим нитроимидазолам.
Лечение, проводимое одновременно у обоих сексуальных партнеров, увеличивает эффективность лечения НГУ.
По данным В. П. Ковалыка (2006), для лечения НГУ, в этиологии которых установлена роль герпетической инфекции, эффективен валацикловир в курсовой дозе 4,0 г (по 2,0 г с интервалом 12 ч). Можно использовать и схемы, предполагающие более длительный прием противовирусных препаратов:
- фамцикловир — по 250 мг 3 раза в сутки в течение 5–10 дней;
- ацикловир — по 200 мг 5 раз в сутки в течение 5–10 дней;
- валацикловир — по 500 мг 2 раза в сутки в течение 5–10 дней.
Если у пациента с НГУ, кроме герпетической инфекции, выявляют и бактериальную, то противогерпетическое лечение назначают как дополнение к антибактериальной терапии. В тех же случаях, когда кроме вирусов при уретритах ничего не обнаруживают, рекомендуется назначать только противовирусную терапию.
Несмотря на правильно проведенную антибиотикотерапию острых НГУ, в 20–69% случаев после окончания лечения через 1–2 нед развивается персистирующий или рецидивирующий уретрит (M. Janier и соавт., 1995; P. J. Horner и соавт., 1999; P. J. Horner и соавт., 2001).
Продолжающийся после лечения уретрита воспалительный процесс является одной из наименее изученных клинических проблем в венерологии. Несмотря на значительные усилия, которые предпринимаются для изучения этого явления, его этиология остается неясной.
Лечение больных хроническим или рецидивирующим НГУ
Поздняя обращаемость пациентов с НГУ, распространение самолечения являются причинами хронизации и осложненного течения заболевания. Терапия больных с длительно протекающими НГУ сопряжена со значительными трудностями в плане достижения клинической эффективности.
Единого подхода к лечению хронического уретрита не существует. Важно клинически и лабораторно подтвердить наличие такого уретрита, поскольку доля пациентов с уретральными симптомами, но без уретрита, достаточно высока.
Схема, предлагаемая Европейским руководством по лечению хронического уретрита: эритромицин — 500 мг 4 раза в день на протяжении 2 нед плюс метронидазол — 2 г однократно или по 400 мг 2 раза в день в течение 5 дней.
По данным K. K. Holmes и соавторов (1998), около 2/3 пациентов после прохождения этого курса лечения избавляются от уретрита, а у оставшейся 1/3 развиваются рецидивы или персистирующие уретриты.
Предлагаются также схемы лечения, отличающиеся большей длительностью приема антибиотиков — от 3 до 6 нед. Однако и они могут оказаться эффективными не для всех пациентов. Врачу важно попытаться найти причину неэффективности антибактериальной терапии и рецидивирования или персистенции уретрита.
Так, например, при длительном существовании в организме C. trachomatis могут менять свой типичный жизненный цикл на атипичный, когда происходит приостановка нормального жизненного цикла хламидий. При этом происходит формирование особых взаимоотношений в системе макро- и микроорганизмов, позволяющих этой системе сосуществовать. Такое явление получило название латенции и персистенции. Клинических проявлений при таком течении инфекции может не быть, как и передачи инфекции от одного сексуального партнера другому.
И антибактериальная терапия на этой стадии может не дать эффекта.
Персистенция хламидий требует особого подхода к больному. Применения одних антибиотиков при этой форме инфекции, как правило, недостаточно, поскольку все эффективные в отношении хламидий антибиотики обладают бактериостатическим действием и способны оказывать свое действие только на размножающиеся бактерии. При лечении таких состояний обычно рекомендуют сочетанную терапию антибиотиками и иммунокорректорами.
Наши наблюдения, основанные на лечении более 1000 больных персистирующим хламидиозом, показывают, что наиболее оптимальным в этих случаях является комбинированная терапия, основанная на сочетании антибиотиков и иммунных препаратов. При антибиотикотерапии используют стандартные для осложненной инфекции курсы и дозировки перечисленных выше антибиотиков. Но начинать лечение желательно с курса иммунотерапии. На основании собственных исследований мы предлагаем следующие варианты предшествующей назначению антибиотиков иммунотерапии:
- полиоксидоний назначается по 6 мг внутримышечно 1 раз в сутки; первые 2 инъекции ежедневно, затем 3 инъекции через день, остальные — 2 раза в неделю, всего на курс — 10 инъекций. После 4-й инъекции начинают курс антибактериальной терапии;
- иммуномакс назначается по 200 МЕ (1 флакон) внутримышечно 1 раз в сутки, 3 инъекции ежедневные, затем перерыв 4 дня и еще 3 ежедневных инъекции, всего на курс — 6 инъекций. После 3-й инъекции начинают курс антибактериальной терапии;
- интерферон α-2β назначается в виде ректальных суппозиториев двумя 5-дневными циклами с интервалом в 2 нед между ними в суммарной дозе 10 млн МЕ на курс. После окончания иммунотерапии проводится курс антибактериальной терапии. Причем оптимальным в этой ситуации оказался курс азитромицина, применяемого по схеме лечения осложненных форм (по 1,0 г на 1, 7 и 14-й дни).
Комбинированная терапия может оказаться эффективной и при рецидивирующих уретритах микоплазменной этиологии. В работе M. M. T. Hadson и соавторов (1998) сообщается о важности иммунологического статуса больного при уреаплазменной инфекции. Использование иммунотропной терапии может быть особенно актуальным при неэффективности хотя бы одного курса противомикробного лечения.
Наши собственные исследования показали, что при выборе иммунотропной терапии особенно высокую эффективность демонстрировал препарат иммуномакс. Этот препарат относится к группе иммуномодуляторов, и показан для коррекции ослабленного иммунитета, лечения и профилактики вирусных и бактериальных инфекций. Схема применения иммуномакса не отличается от способа его применения при рецидивирующей хламидийной инфекции.
Таким образом, адекватная, т. е. основанная на результатах клинико-лабораторных исследований и существующих рекомендациях, антибактериальная терапия позволяет достичь положительного эффекта при НГУ.
М. А. Гомберг, доктор медицинских наук, профессор А. М. Соловьев, кандидат медицинских наук, доцент В. П. Ковалык, кандидат медицинских наук ЦНИКВИ, МГМСУ, Москва
Правила подготовки пациента
У мужчин: из уретры.Стандартные условия:
В течение рабочего дня ДЦ.
Важно:
На протяжении суток перед забором материала не применять препаратов местного значения, на протяжении 2-х часов воздержаться от мочеиспускания.
Возможно:
отклонения от стандартных условий по согласованию с врачом.
Вы можете добавить данное исследование в корзину на этой странице
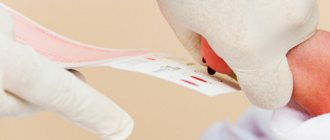
Проведение процедуры взятия мазка
В уретральный канал на глубину около 3 сантиметров вводится специальный зонд или тампон, им проводится забор мазка. При этом мужчина может испытывать неприятные ощущения, боль в головке полового члена, что может сохранятся на протяжении некоторого времени после процедуры взятия материала для анализа. Если боли не проходят, появились гнойные или кровянистые выделения из уретры, следует срочно обратиться к врачу.
При необходимости врач перед забором мазка может назначить массаж предстательной железы через анальное отверстие или мочеиспускательный канал с помощью специального зонда.
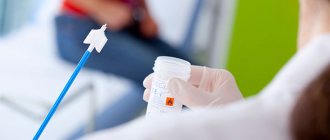
В качестве материала для посева используют такие биологические жидкости, как:
- Моча;
- Эякулят;
- Секрет предстательной железы;
- Выделение из мужской уретры.
Полученные материалы помещают в питательную среду. По истечению недели будут готовы результаты бак посева из уретры. Помимо вида микроорганизма лаборанты выявят те активные лекарственные вещества, к которым данный возбудитель инфекции чувствителен.
Интерпретация:
- лейкоциты (нейтрофилы й лимфоциты): свежий уретрит или обострение хронического уретрита;эозинофилов (свыше 5-10 %) — аллергический уретрит;клетки эпителия (при небольшом числе лейкоцитов): хронический уретрит с метаплазией зпителия (десквамативный уретрит) или лейкоплакия уретры;эритроциты (с лейкоцитами и эпителиальными клетками): травматический уретрит, опухоль уретры, кристаллурия, изъязвление слизистой оболочки и др.;липоидные зёрна: простаторея;сперматозоиды: сперматорея;слизь без форменных элементов: уретрорея;скопления мелких полиморфных палочек на клетках эпителия (ключевые клетки) при небольшом количестве полинуклеарных нейтрофилов: уретрит, обусловленный Corynebacterium vaginale;ключевые клетки, бактерии, единичные полинуклеарные нейтрофилы: бактериорея.
Образец результата (PDF)