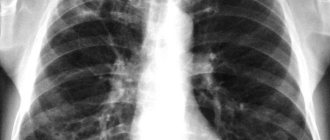
Инфильтративный туберкулез легких
Первичное инфицирование микобактериями туберкулеза и скрытое течение туберкулёзной инфекции. Первичное заражение человека МБТ обычно происходит аэрогенным путем. Другие пути проникновения — алиментарный, контактный и трансплацентарный — встречаются значительно реже.
Система дыхания защищена от проникновения микобактерий мукоцилиарным клиренсом (выделение бокаловидными клетками дыхательных путей слизи, которая склеивает поступившие микобактерии, и дальнейшая элиминация микобактерий с помощью волнообразных колебаний мерцательного эпителия). Нарушение мукоцилиарного клиренса при остром и хроническом воспалении верхних дыхательных путей, трахеи и крупных бронхов, а также под воздействием токсических веществ делает возможным проникновение микобактерий в бронхиолы и альвеолы, после чего вероятность инфицирования и заболевания туберкулёзом значительно увеличивается. Возможность заражения алиментарным путём обусловлена состоянием стенки кишечника и его всасывающей функции.
Возбудители туберкулёза не выделяют какой-либо экзотоксин, который мог бы стимулировать фагоцитоз. Возможности фагоцитоза микобактерий на этом этапе ограничены, поэтому присутствие в тканях небольшого количества возбудителя проявляется не сразу. Микобактерии находятся вне клеток и размножаются медленно, и ткани некоторое время сохраняют нормальную структуру. Это состояние называется «латентный микробизм». Независимо от начальной локализации они с током лимфы попадают в регионарные лимфатические узлы, после чего лимфогенно распространяются по организму — происходит первичная (облигатная) микобактериемия. Микобактерии задерживаются в органах с наиболее развитым микроциркуляторным руслом (лёгкие, лимфатические узлы, корковый слой почек, эпифизы и метафизы трубчатых костей, ампуллярно-фимбриональные отделы маточных труб, увеальный тракт глаза). Поскольку возбудитель продолжает размножаться, а иммунитет ещё не сформировался, популяция возбудителя значительно увеличивается. Тем не менее, в месте скопления большого числа микобактерий начинается фагоцитоз. Сначала возбудителей начинают фагоцитировать и разрушать полинуклеарные лейкоциты, однако безуспешно — все они гибнут, вступив в контакт с МБТ, из-за слабого бактерицидного потенциала.
Затем к фагоцитозу МБТ подключаются макрофаги. Однако МБТ синтезируют АТФ-положительные протоны, сульфаты и факторы вирулентности (корд-факторы), в результате чего нарушается функция лизосом макрофагов. Образование фаголизосомы становится невозможным, поэтому лизосомальные ферменты макрофагов не могут воздействовать на поглощённые микобактерии. МБТ располагаются внутриклеточно, продолжают расти, размножаться и всё больше повреждают клетку-хозяина. Макрофаг постепенно погибает, а микобактерии вновь попадают в межклеточное пространство. Этот процесс называется «незавершённым фагоцитозом».
Приобретённый клеточный иммунитет В основе приобретённого клеточного иммунитета лежит эффективное взаимодействие макрофагов и лимфоцитов. Особое значение имеет контакт макрофагов с Т-хелперами (CD4+) и Т-супрессорами (CD8+). Макрофаги, поглотившие МБТ, экспрессируют на своей поверхности антигены микобактерий (в виде пептидов) и выделяют в межклеточное пространство интерлейкин-1 (ИЛ-1), который активирует Т-лимфоциты (CD4+). В свою очередь Т-хелперы (CD4+) взаимодействуют с макрофагами и воспринимают информацию о генетической структуре возбудителя. Сенсибилизированные Т-лимфоциты (CD4+ и CD8+) выделяют хемотаксины, гамма-интерферон и интерлейкин-2 (ИЛ-2), которые активируют миграцию макрофагов в сторону расположения МБТ, повышают ферментативную и общую бактерицидную активность макрофагов. Активированные макрофаги интенсивно вырабатывают активные формы кислорода и перекись водорода. Это так называемый кислородный взрыв; он воздействует на фагоцитируемый возбудитель туберкулёза. При одновременном воздействии L-аргинина и фактора некроза опухолей-альфа образуется оксид азота NO, который также обладает антимикробным эффектом. В результате всех этих процессов разрушительное действие МБТ на фаголизосомы ослабевает, и бактерии разрушаются лизосомальными ферментами. При адекватном иммунном ответе каждое последующее поколение макрофагов становится всё более иммунокомпетентным. Выделяемые макрофагами медиаторы активируют также B-лимфоциты, ответственные за синтез иммуноглобулинов, однако их накопление в крови на устойчивость организма к МБТ не влияет. Но выработка B-лимфоцитами опсонирующих антител, которые обволакивают микобактерии и способствуют их склеиванию, является полезной для дальнейшего фагоцитоза.
Повышение ферментативной активности макрофагов и выделение ими различных медиаторов может вести к появлению клеток повышенной чувствительности замедленного типа (ПЧЗТ) к антигенам МБТ. Макрофаги трансформируются в эпителиоидные гигантские клетки Лангханса, которые участвуют в ограничении зоны воспаления. Образуется экссудативно-продуктивная и продуктивная туберкулёзная гранулёма, образование которой свидетельствует о хорошем иммунном ответе на инфекцию и о способности организма локализовать микобактериальную агрессию. На высоте гранулематозной реакции в гранулеме находятся Т-лимфоциты (преобладают), B-лимфоциты, макрофаги (осуществляют фагоцитоз, выполняют аффекторную и эффекторную функции); макрофаги постепенно трансформируются в эпителиоидные клетки (осуществляют пиноцитоз, синтезируют гидролитические ферменты). В центре гранулёмы может появиться небольшой участок казеозного некроза, который формируется из тел макрофагов, погибших при контакте с МБТ.
Реакция ПЧЗТ появляется через 2-3 недели после инфицирования, а достаточно выраженный клеточный иммунитет формируется через 8 недель. После этого размножение микобактерий замедляется, общее их число уменьшается, специфическая воспалительная реакция затихает. Но полной ликвидации возбудителя из очага воспаления не происходит. Сохранившиеся МБТ локализуются внутриклеточно (L-формы) и предотвращают формирование фаголизосомы, поэтому недоступны для лизосомальных ферментов. Такой противотуберкулёзный иммунитет называется нестерильным. Оставшиеся в организме МБТ поддерживают популяцию сенсибилизированных Т-лимфоцитов и обеспечивают достаточный уровень иммунологической активности. Таким образом, человек может сохранять МБТ в своем организме длительное время и даже всю жизнь. При ослаблении иммунитета возникает угроза активизации сохранившейся популяции МБТ и заболевания туберкулёзом.
Приобретенный иммунитет к МБТ снижается при СПИДе, сахарном диабете, язвенной болезни, злоупотреблении алкоголем и длительном применении наркотиков, а также при голодании, стрессовых ситуациях, беременности, лечении гормонами или иммунодепрессантами.
В целом риск развития туберкулёза у впервые инфицированного человека составляет около 8 % в первые 2 года после заражения, постепенно снижаясь в последующие годы.
Возникновение клинически выраженного туберкулёза В случае недостаточной активации макрофагов фагоцитоз неэффективен, размножение МБТ макрофагами не контролируется и потому происходит в геометрической прогрессии. Фагоцитирующие клетки не справляются с объёмом работы и массово гибнут. При этом в межклеточное пространство поступает большое количество медиаторов и протеолитических ферментов, которые повреждают прилежащие ткани. Происходит своеобразное «разжижение» тканей, формируется особая питательная среда, способствующая росту и размножению внеклеточно расположенных МБТ.
Большая популяция МБТ нарушает баланс в иммунной защите: количество Т-супресоров (CD8+) растёт, иммунологическая активность Т-хелперов (CD4+) падает. Сначала резко усиливается, а затем ослабевает ПЧЗТ к антигенам МБТ. Воспалительная реакция приобретает распространённый характер. Повышается проницаемость сосудистой стенки, в ткани поступают белки плазмы, лейкоциты и моноциты. Формируются туберкулёзные гранулёмы, в которых преобладает казеозный некроз. Усиливается инфильтрация наружного слоя полинуклеарными лейкоцитами, макрофагами и лимфоидными клетками. Отдельные гранулёмы сливаются, общий объём туберкулёзного поражения увеличивается. Первичное инфицирование трансформируется в клинически выраженный туберкулёз.
При каких заболеваниях «матовое стекло» проявляется на томограммах?
По данным кафедры лучевой диагностики ММА им. Сеченова, картину «матовости» чаще всего дают пневмонии (вирусные, бактериальные, грибковые), однако инфильтрация легких характерна и для других патологических состояний. Вот только некоторые из них:
- Альвеолярный протеиноз;
- Пневмонит;
- Кровоизлияние;
- Гранулематозы;
- Альвеолярный отек;
- Аллергический альвеолит;
- Туберкулез;
- Медикаментозное поражение легких;
- Инфаркт легкого;
- Вирусная инфекция;
- Дерматомиозит;
- Опухоли;
- Ревматоидный артериит;
- Респираторный бронхиолит с ИЗЛ;
- Синдром Съегрена;
- Синдром Гудпасчера;
- Склеродермия.
Оценивая данные КТ легких, врач-рентгенолог дифференцирует заболевания по специфической картине «матовых стекол»: их количеству, локализации, наличию других признаков, по которым возможно определить причину патологических изменений ткани легких. Например, для двусторонней вирусной пневмонии характерно наличие «матовых стекол», расположенных периферически в нижних и задних отделах легких. В более поздней стадии наблюдается консолидация очагов инфильтрации с утолщением перегородок альвеол.
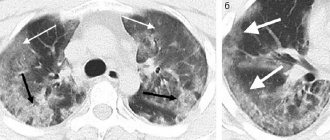
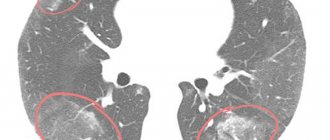
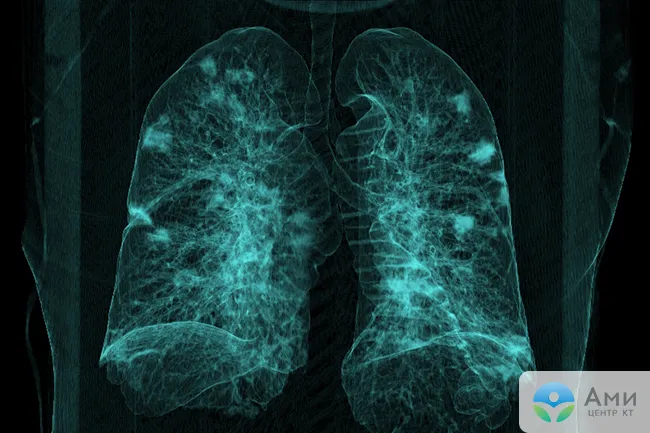
«Матовые стекла» при туберкулезе могут быть расположены рядом с бронхами или диссеминированы — в этом случае наблюдается множество маленьких светлых участков (инфильтратов), хаотично расположенных во всей полости легких. Также при туберкулезе на КТ легких можно обнаружить характерные фиброзные тяжи, ведущие к корню легкого — это перибронхиальное воспаление, признаки лимфостаза с увеличением лимфатических узлов. Единичные участки «матового стекла» малого размера без четкого паттерна какого-либо заболевания могут указывать на новообразование, развивающийся фиброз, аденокарциному (рак) легких.
Иногда «матовые стекла» указывают на сосудистые патологии, которые приводят к сдавливанию альвеолярного пространства. У пациентов с ожирением могут появится в гравитационно-зависимых (нижних) областях легких под воздействием лишнего веса. У здоровых пациентов эффект «матового стекла» может проявиться на томограммах в случае, если сканирование грудной клетки проведено на выдохе (правильно — на глубоком вдохе).
Не принимая в расчет эти погрешности и говоря об истинном синдроме «матового стекла» на КТ легких, отметим, что это признак нефункциональных участков легких. В норме уплотнений и препятствий для дыхания быть не должно, а легочная ткань представлена на томограммах однородным темным цветом. Очень редко «матовые стекла» указывают на индивидуальные особенности организма пациента, например, на нетипичное расположение диафрагмы у новорожденных. Но это единичные случаи, поэтому давайте рассмотрим наиболее распространенные паттерны заболеваний, при которых на томографии встречаются «матовые стекла».
«Матовые стекла» на КТ при пневмонии
Чаще всего «матовое стекло» на КТ проявляется при воспалении легких, причем это может быть абсолютно любая пневмония: вирусная, бактериальная, с атипичным развитием симптомокомплекса, очень редкая интерстициальная и так далее. Поскольку спектр возбудителей пневмонии чрезвычайно широк, а дифференцировать заболевания легких по одному эффекту «матового стекла» не всегда представляется возможным, пациенту рекомендуется лабораторная диагностика — анализ крови или отделяемого из дыхательных путей на предмет микоплазм, пневмококков, коронавируса и других возбудителей.
Общим признаком острых пневмоний на КТ является наличие инфильтратов («матовых стекол») разной формы и протяженности. «Матовые стекла» расположены вокруг очагов или диффузно, как при туберкулезе. Однако в отличие от туберкулеза, их размер обычно больше, есть тенденция к консолидации инфильтратов и образованию рисунка по типу «булыжной мостовой». В отдельных случаях визуализируются просветы бронхов, содержащих газ. Это называется синдромом «воздушной бронхографии». В сочетании с эффектом «матового стекла», он также относится к явным признакам пневмонии.
Для пневмонии, вызванной коронавирусом COVID-19, характерно периферическое расположение очагов поражения под плеврой. Наиболее уязвимы билатеральные нижние доли и задние отделы легких. Отмечается тенденция к консолидации «матовых стекол» и утолщению перегородок альвеол, иногда — признаки фиброза легких.
Тяжелым формам коронавирусной пневмонии сопутствует острый респираторный дистресс-синдром. ОРДС — это обширное двухстороннее воспаление, при котором наблюдается множество инфильтратов и отек легких. На томограммах фрагментарные участки «матового стекла» кортикальной формы присутствуют с двух сторон и имеют вид «лоскутного одеяла».
При пневмоцистной пневмонии, вызванной дрожжеподобным грибом Pneumocystis Jirovecii, наблюдается несколько иная картина. Участки уплотнения легких по типу «матового стекла» обычно расположены с двух сторон симметрично (но иногда диффузно и неравномерно). Уплотнения преобладают в прикорневых областях легких, а диффузные изменения — в верхних и нижних отделах. Для пневмоцистной пневмонии, как и для вирусной, ассоциированной с COVID-19, характерны эффект консолидации и симптом «лоскутного одеяла», но на томограммах легких видны и другие признаки: воздушные кисты, пневмоторакс.
Отдельную группу заболеваний представляют идиопатические интерстициальные пневмонии, причину которых не удается установить. Помимо «матового стекла» на сканах КТ легких можно обнаружить симптом «сотового легкого», бронхоэктазы, ретикулярные изменения. Идиопатические пневмонии требуют гистологического обследования.
На основании данных компьютерной томографии легких и анамнеза пациента врач-рентгенолог сможет определить поражение легких, характерное для пневмонии. В рамках дифференциальной диагностики учитывается плотность и форма «матовых стекол», их количество, в целом оценивается рисунок. Однако определить возбудителя пневмонии и тактику лечения можно после дополнительной лабораторной диагностики.