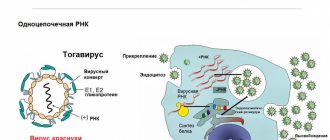
Токсоплазма (Toxoplasma gondii) – это кокцидия, являющаяся самым распространенным внутриклеточным паразитом теплокровных животных.
Инвазирование теплокровных млекопитающих происходит при проглатывании любой из трех стадий T. gondii (спорозоита, тахизоита, брадизоита) и трансплацентарно. Возможна передача возбудителя котятам с молоком инвазированной матери.
Завершение половой фазы жизненного цикла токсоплазм происходит только в желудочно-кишечном тракте кошек (энтероэпителиальный цикл). По ее завершении с фекалиями выделяются цисты, устойчивые к факторам внешней среды. Через 1-3 дня после контакта с кислородом и при благоприятной температуре и влажности в цистах развиваются спорозоиты, данный процесс называется споруляцией. После проглатывания ооцист в тонком кишечнике кошек или промежуточных хозяев паразита из них выходят спорозоиты. В период активной инфекции в результате размножения спорозоитов в эпителиальных тканях образуются тахизоиты, которые мигрируют в кровь и лимфу.
T. gondii может проникать в большинство клеток млекопитающих, в которых проходит бесполое размножение паразита вплоть до разрушения клетки. При наличии корректного иммунного ответа репликация тахизоитов замедляется, и появляются медленно делящиеся брадизоиты, которые находятся внутри цист в экстраинтестинальных тканях. Данные тканевые цисты могут быстро образовываться в центральной нервной системе, мышечной ткани и внутренних органах. Брадизоиты сохраняют жизнеспособность в тканевых цистах на протяжении всей жизни хозяина. Серопревалентность к T. gondii варьирует в зависимости от образа жизни животного, в целом наблюдается прямая корреляция серопревалентности и возраста, что связана с ростом риска контакта с возбудителем. Также отмечается зависимость данного показателя от возможности доступа животных за пределы помещений, где они могут контактировать с инвазированными промежуточными хозяевами.
Развитие клинического токсоплазмоза зависит от особенностей возбудителя и иммунного ответа хозяина. Некоторые штаммы обладают более высокой патогенностью, другие отличаются аффинностью к определенным типам тканей, как, например, патологии глаз у кошек с токсоплазмозом. При недостаточной эффективности иммунного ответа после первичного инвазирования происходит чрезвычайно интенсивная репликация тахизоитов, вызывающая некроз тканей, который является основной причиной наблюдаемых патологических нарушений. Заболевания, сопровождаемые иммуносупрессией, такие как инфекция FIV, могут вызывать активацию токсоплазмоза. У подавляющего большинства кошек, инвазированных T. gondii, никогда не происходит развития клинических симптомов. У собак инфекция проявляется расстройствами со стороны респираторной, нервно-мышечной систем и желудочно-кишечного тракта. Легкая форма заболевания часто протекает бессимптомно. Генерализованный токсоплазмоз чаще всего встречается у собак с иммуносупрессией, например, при чуме плотоядных, либо получающих лечение циклоспоринами для предотвращения отторжения трансплантататов.
Диагностика токсоплазмоза должна осуществляться комплексно, с учетом клинических признаков и результатов серологических и других видов исследований. Титр IgM будет возрастать в первые две недели после заражения животного и может сохраняться до 12-15 недель с момента заражения. Нарастание титра антител класса IgM без увеличения титра IgG свидетельствует о фазе активного заражения. Выработка антител класса IgG начинается с третьей недели от начала заболевания животного. Этот класс иммуноглобулинов может сохраняться и осуществлять защитную функцию в течение нескольких лет, а иногда и пожизненно. Поэтому при подозрении на инфицирование важно исследовать парные сыворотки, взятые с промежутком в несколько недель. Возрастание титра антител в повторном тесте будет подтверждать наличие заболевания. IgG (но не IgM) могут передаваться плодам от матери. Обнаружение высоких титров антител класса IGg к Toxoplasma gondii у новорожденных животных может свидетельствовать о заражении матери во время беременности и трансплацентарной передаче инфекции.
Комплексы с этим исследованием
Планирование беременности. Диагностика инфекций 14 анализов для будущих мам 8 620 Р Состав
Невынашивание беременности Выявление основных причин невынашивания беременности 40 070 Р Состав
Планирование ЭКО Обследование для предварительной подготовки женщины к процедуре ЭКО 12 990 Р Состав
В ДРУГИХ КОМПЛЕКСАХ
- TORCH-инфекции. Авидность антител IgG 5 920 Р
- Обследование во время беременности. 1 триместр 16 690 Р
- Вступление в ЭКО 23 020 Р
Результат исследования
Тест качественный. Результат выдается в терминах «отрицательно», «сомнительно», «положительно».
Положительно – антитела класса IgG к Toxoplasma gondii обнаружены. Это может свидетельствовать о начальном периоде первичной инфекции, либо о об инфекции, перенесенной ранее. Для дифференциации данных состояний, целесообразно провести повторное исследование через 3-4 недели. Нарастание полученного коэффициента (КП) в 4 и более раз, свидетельствует об активной инфекции.
Сомнительно – полученный результат находится на границе порогового значения, которое не позволяет достоверно (с вероятностью более 95%) отнести результат к «Положительно» или «Отрицательно». Следует учитывать, что такой результат возможен при очень низком уровне антител, который может иметь место, в частности, в начальный период заболевания. В зависимости от клинической ситуации может быть полезным повторное исследование уровня антител через 3-4 недели для оценки динамики. При получении повторного сомнительного результата, проба считается отрицательной, то есть антитела не обнаружены.
Отрицательно — антитела класса IgG в исследуемом образце не обнаружены. Это может свидетельствовать об отсутствии контакта животного с Toxoplasma gondii или о раннем инфицировании. В зависимости от клинической ситуации может быть полезным повторное исследование уровня антител через 3-4 недели.
Подробное описание исследования
Toxoplasma gondii — внутриклеточный паразит, принадлежащий к царству простейших. Существует три основных инфекционных стадии жизненного цикла этого патогена: спорозоиты, тахизоиты и брадизоиты.
Кошки и другие представители семейства кошачьих служат конечным хозяином токсоплазмы. Паразит обитает в клетках их пищеварительной системы. Заражение кошек осуществляется при употреблении инфицированного мяса.
Обитая в кишечнике этих животных, токсоплазма продуцирует яйца (ооцисты), устойчивые к воздействию внешней среды. В таком виде паразит выделяется с фекалиями кошек. Попадание его в желудочно-кишечный тракт человека, который является промежуточным хозяином данного паразита, происходит при контакте немытых рук или поверхностей с ротовой полостью. Это возможно в случае нарушения гигиены:
– во время очистки кошачьего туалета; – после разделки инфицированного мяса; – контакта с почвой, содержащей яйца токсоплазмы.
Попадание в кишечник человека способствует трансформации паразита в тахизоиты. Тахизоиты — это быстро воспроизводящаяся форма паразита, которая характеризует острую стадию инфекции. В таком виде токсоплазма распространяется по всему организму с током крови, попадая в том числе в мышцы, головной мозг. Впоследствии данный паразит превращается в медленно воспроизводящуюся форму — брадизоиты. Именно она превалирует при хронической инфекции.
Цисты в тканях, содержащие жизнеспособные брадизоиты, сохраняются годами в течение всей жизни человека. Мозг и мышцы служат наиболее частыми локализациями хронической скрытой инфекции, хотя могут обнаруживаться в легких, печени, почках и других внутренних органах.
Заражение токсоплазмозом не имеет характерных симптомов и обычно похоже на проявления острой респираторной инфекции или мононуклеоза. Ухудшение самочувствия краткосрочно, иногда заболевание протекает в стертой форме или бессимптомно. Инфекция подавляется иммунной системой, но возбудитель может оставаться в организме пожизненно. Реактивация токсоплазмоза наступает в случае подавления иммунитета, например, при заражении вирусом иммунодефицита человека.
Инфицирование токсоплазмой несет опасность для беременных женщин. У части из них данный паразит способен преодолевать плацентарный барьер и поражать плод. В первом триместре беременности риск воздействия на плод меньше (около 20%), в то время как к концу третьего триместра достигает 80%. Однако заражение на ранних сроках беременности приводит к более тяжелым последствиям: самопроизвольному аборту, гидроцефалии или умственной отсталости ребенка. В то же время в последнем триместре большинство случаев являются более легкими, но иногда приводят к поражению глаз и слепоте.
Заражение токсоплазмой приводит к образованию иммунной системой антител класса М, затем — класса G. Последние отражают контакт с возбудителем в сроки более месяца. Анализ количества IgG необходим для оценки иммунитета к токсоплазме, что особенно важно для людей с нарушенным иммунитетом и при беременности.
УЗИ Гинеколог
Токсоплазмоз – широко распространенная паразитарная инфекция, характеризующаяся многообразием клинических проявлений и значительной вариабельностью течения процесса – от бессимптомного носительства до тяжелых и летальных форм болезни. Особенностью токсоплазмоза является возможность инфицирования плода во время внутриутробного развития с возникновением тяжелых аномалий развития. В различных регионах мира инфицированность населения токсоплазмозом колеблется от 10 до 90%.
ЭТИОЛОГИЯ
Возбудитель токсоплазмоза – Toxoplasma gondii – внутриклеточный паразит, размером 4–7 мкм, способный паразитировать в организме человека и животных практически во всех органах и тканях.
Основной источник инфекции – представители семейства кошачьих, в организме которых возбудитель проходит полный цикл развития (тканевой и кишечный) и в виде ооцист с фекалиями выводится наружу. За 10–15 дней болезни инфицированная кошка выделяет во внешнюю среду около 2 миллиардов ооцист. В почве ооцисты могут сохранять свою жизнеспособность до 1,5–2,0 лет.
Пути заражения токсоплазмозом:
• Пероральный – основной и наиболее частый способ заражения – заглатывание цист, ооцист при употреблении сырых или недостаточно термически обработанных мясных продуктов с находящимися в них цистами токсоплазм, плохо вымытой зелени, овощей, фруктов, загрязненных ооцистами возбудителя.
• Перкутантный – при ранении кожи, повреждении слизистых оболочек у работников скотобоен, мясокомбинатов, ветеринаров.
• Трансплацентарный – при возникновении паразитемии во время беременности.
• Гемотрансфузионный, трансплантационный – при переливании инфицированной крови и пересадке органов.
ПАТОГЕНЕЗ
При пероральном заражении возбудители внедряются в эпителиальные клетки тонкого кишечника, где они размножаются, проникают затем в региональные лимфатические узлы, а из них с током лимфы – в кровь. Диссеминация возбудителя приводит к поражению самых различных органов и тканей. Формирование иммунитета способствует исчезновению возбудителя из крови, прекращается его размножение в клетках. Образуются истинные тканевые цисты, которые могут длительно, десятилетиями, сохраняться в организме.
КЛИНИКА
У большей части инфицированных Toxoplasma gondii (95–99%) клинические проявления заболевания отсутствуют. Наблюдается носительство паразита, сопровождающееся стабильным уровнем концентрации иммуноглобулинов класса G (Тoxo-IgG) в крови. Носительство не требует каких-либо терапевтических мероприятий, а носитель должен расцениваться как практически здоровый человек.
В то же время возможны и клинические выраженные варианты течения первичной инфекции (как правило, возникающие у лиц с нарушением иммунитета) с развитием энцефалита, миокардита, миозита, увеита (хориоретинита), формированием хронического токсоплазмоза.
Возможна реактивация латентной инфекции (1–5% от числа инфицированных) под влиянием факторов, способных вызывать иммуносупрессию (перенесенные грипп, ОРЗ, длительное лечение цитостатиками, глюкокортикоидами, лучевая терапия, психоэмоциональный стресс).
Весьма актуальна проблема генерализации латентного токсоплазмоза у ВИЧ-инфицированных с развитием тяжелого некротического энцефалита с большой вероятностью летального исхода. Токсоплазмоз является характерной и часто наблюдаемой СПИД-ассоциированной инфекцией, приводящей к поражению различных органов и систем у больных.
TОКСОПЛАЗМОЗ У БЕРЕМЕННЫХ
Токсоплазмоз входит в группу ТОRСН-инфекций, считающихся потенциально опасными для внутриутробного развития плода.
Согласно современным представлениям, внутриутробное поражение плода при токсоплазмозе может происходить лишь в случае первичного инфицирования во время беременности. Во время паразитемии возможно инфицирование плаценты и передача Toxoplasma gondii плоду. Обычно в таких случаях возникает угроза выкидыша; современные высокоэффективные способы лечения угрожающих выкидышей позволяют сохранить данную беременность, однако она может закончиться рождением ребенка с тяжелой внутриутробной инфекцией.
В случае первичного инфицирования беременной риск внутриутробного заражения плода увеличивается примерно от 17% в I триместре (проницаемость плаценты минимальна) до 80% – в III триместре (проницаемость плаценты повышается). Тяжесть поражения плода находится в зависимости от стадии внутриутробного развития. Инцифирование в I–II триместре беременности приводит к наиболее тяжелым последствиям (табл. 1).
| Таблица 1 Риск инфицирования плода при первичном токсоплазмозе | ||
| Срок беременности, недели | Риск заражения, % | Исход |
| 0–8 | 17 | Тяжелые аномалии развития |
| 8–18 | 25 | Поражение ЦНС (гидро-, микроцефалия, кальцификаты в тканях мозга, эписиндром), хориоретинит, микрофтальм |
| 18–24 | 65 | Нарушение функций различных органов (гепатоспленомегалия, желтуха, анемия, тромбоцитопения) |
| 24–40 | 80 | Субклинические проявления болезни с манифестацией через несколько лет (глухота, хориоретинит, нарушение психомоторного развития) |
Таким образом, важно определить время инфицирования беременной: задолго до, непосредственно перед либо во время беременности.
Уверенно можно говорить об инфицировании в период беременности при наличии комплекса следующих показателей: а) определение сероконверсии; б) двукратное нарастание концентрации специфических IgG при исследовании парных сывороток, взятых с интервалом в 2–3 недели и одновременное наличие специфических IgM, IgA; в) присутствие низкоавидных специфических IgG.
Чем позже беременная женщина обращается в женскую консультацию и чем позже проводится первичное серологическое обследование, тем менее определенный ответ может быть дан по срокам инфицирования.
Только при подтвержденном инфицировании в I триместре беременности, когда риск рождения ребенка с грубыми органическими поражениями ЦНС и глаз наибольший, можно ставить вопрос о прерывании беременности по медицинским показаниям! Женщины, заразившиеся во II и III триместре беременности, подлежат лечению.
Давая рекомендации по последующим беременностям, необходимо учитывать, что ребенок с врожденным токсоплазмозом может родиться только один раз в жизни. При последующих беременностях женщина может не опасаться рождения больного врожденным токсоплазмозом ребенка.
Проконсультироваться с врачом и пройти лабораторное обследование на все ТORCH-инфекции женщине необходимо за 2–3 месяца до планируемой беременности, поскольку только в этом случае имеется возможность выделить группу риска (серонегативных) и предпринять соответствующие лечебные или профилактические меры.
ЛАБОРАТОРНАЯ ДИАГНОСТИКА
Из-за отсутствия патогномоничных симптомов постановка диагноза первичного токсоплазмоза на основании клинической картины практически исключена, поэтому решающую роль приобретают методы лабораторной диагностики: определение специфических антител и выявление самого возбудителя.
В настоящее время для диагностики токсоплазмоза наиболее широко используются серологические методы, в основном ИФА, поскольку методы выявления Toxoplasma gondii имеют ограничения – возбудитель присутствует в крови непродолжительное время.
При попадании токсоплазм в организм человека через 7–14 дней начинается первичный гуморальный иммунный ответ: продуцируются специфические IgM (Toxo-IgM). Максимальный уровень концентрации Toxo-IgM достигается к 20–30-му дню от начала инфицирования. Полное их исчезновение в большинстве случаев (около 70%) происходит в течение 3–4 месяцев, однако возможно присутствие Toxo-IgM и более длительное время –до 1 года и более (около 10% случаев).
Реинфекция токсоплазмами на фоне ранее приобретенного здорового носительства также может приводить к появлению Тохо-IgM. В настоящее время нет подтверждённых данных, что Тохо-IgM могут выявляться при реактивации латентной инфекции, хроническом токсоплазмозе.
Toxo-IgА начинают выявляются в крови через 14 дней с момента инфицирования, достигая максимальной концентрации через месяц. Toxo-IgА обычно исчезают через 6 месяцев (около 90% случаев), но могут персистировать в отдельных случаях более 1 года. Следовательно, обнаружение Toxo-IgM и Toxo-IgА не является строгим показателем «свежей» инфекции, а свидетельствует только о первичном инфицировании в пределах предыдущих 12 месяцев.
Уровень концентрации специфических иммуноглобулинов класса G (Toxo-IgG) в первые 2–3 месяца заболевания нарастает, в течение года их концентрация остается стабильной, а затем несколько снижается.
Для получения более точных данных по срокам заражения и длительности инфекционного процесса используют определение индекса авидности Toxo-IgG. Авидность – характеристика прочности связывания специфических антител с соответствующими антигенами. При формировании иммунного ответа сначала образуются Toxo-IgG, обладающие низкой авидностью, т.е. достаточно слабо связывающиеся с антигеном.
Индекс авидности (ИА) Toxo-IgG в первые 2–6 месяцев заболевания нарастает. Если в крови, наряду со специфическими Toxo-IgМ и Toxo-IgА, обнаруживаются IgG с низкой авидностью, то это указывает на острую стадию первичной инфекции. Наличие же Toxo-IgМ, Тохо-IgA и высокоавидных IgG предполагает длительную персистенцию этих иммуноглобулинов после завершения острой стадии первичной инфекции либо вторичный иммунный ответ в случае реинфекции T. gondii. Определение высокоавидных IgG при отсутствии IgM свидетельствует о пастинфекции.
Обнаружение низкоавидных IgG при отрицательном результате на Toxo-IgM может иметь место при сроках инфицирования более 3 месяцев. В таких случаях необходимо определять в динамике увеличение индекса авидности.
У иммунодефицитных больных повышение концентрации Toxo-IgG и выявление Toxo-IgM и Toxo-IgА наблюдается редко. Доказательством наличия инфекции может стать выявление T. gondii, в частности, ДНК возбудителя методом ПЦР.
Определить вероятный срок инфицирования T. gondii позволяет анализ полного спектра серологических маркеров токсоплазмоза:
результатов выявления специфических IgM, IgA,
определения индекса авидности IgG и концентрации IgG в динамике (табл. 2).
ДИАГНОСТИКА ВРОЖДЕННОГО ТОКСОПЛАЗМОЗА
При подозрении на врожденный токсоплазмоз серологическое обследование матери и ребенка в течение первого года жизни ребенка следует проводить не менее 4–6 раз. Как известно, иммуноглобулины класса G (в отличие от IgM) могут передаваться плоду трансплацентарно. При отсутствии инфицирования плода к 4–6 мес. после рождения концентрация Тохо-IgG резко снижается вследствие распада материнских антител. В случае инфицирования концентрация Тохо-IgG нарастает, однако в первом полугодии жизни «маскируется» наличием материнских антител.
Наиболее точным критерием наличия врожденного токсоплазмоза является обнаружение Тохо-IgM в сыворотке крови ребенка. Однако вследствие незрелости иммунной системы новорожденного и низкой продукции IgM, а также возможности прохождения острой стадии инфекции внутриутробно (при инфицировании в ранние сроки беременности) факт инфицирования не всегда подтверждается наличием Тохо-IgM в пуповинной крови. Таким образом, отсутствие Тохо-IgM у новорожденных и детей раннего возраста не дает основания исключить внутриутробное заражение токсоплазмозом.
Поскольку IgA не проходят через плаценту, определение Тохо-IgA может помочь в диагностике эмбриональной инфекции, неонатального и постнатального мониторинга врожденного токсоплазмоза. Решающее значение имеет анализ клинического состояния ребенка, акушерский анамнез матери и подтверждение диагноза выявлением ДНК T. gondii в крови и моче ребенка методом ПЦР.
Средства иммунопрофилактики токсоплазмоза к настоящему времени не разработаны, поэтому только определение иммунного статуса беременных женщин в отношении токсоплазменной инфекции позволяет контролировать развитие очень опасного для плода первичного инфицирования T. gondii.
Авидность (лат. — avidity) характеристика прочности связи специфических антител с соответствующими антигенами. В ходе иммунного ответа организма на проникновение инфекционного агента стимулированный клон лимфоцитов начинает вырабатывать сначала специфические IgM-антитела, а несколько позже и специфические IgG-антитела. IgG-антитела обладают поначалу низкой авидностью, то есть достаточно слабо связывают антиген. Затем развитие иммунного процесса постепенно (это могут быть недели или месяцы) идет в сторону синтеза лимфоцитами высокоавидных IgG-антител, более прочно связывающихся с соответствующими антигенами. Высокая авидность специфических IgG-антител позволяет исключить недавнее первичное инфицирование.
Подтверждение или исключение факта недавнего первичного инфицирования Toxoplasma gondii особенно важно при обследовании беременных женщин, поскольку риск патологии развития плода существенно увеличен при остром первичном инфицировании во время беременности, по сравнению с хронической инфекцией и реактивацией латентной инфекции. Поэтому постоянно идет поиск новых диагностических подходов, позволяющих максимально достоверно оценить стадию и форму инфекционного процесса. Использование авидности IgG-антител в качестве индикатора срока первичного инфицирования, впервые предложенное финскими исследователями (Hedman K. M. с соавт.,1989), в настоящее время в ряде стран введено в практику серологических исследований на TORCH-инфекции. Так, во Франции, где, как и в России, проблема токсоплазмоза по-прежнему актуальна, этот тест входит в обязательный алгоритм обследования при подозрении на токсоплазмоз у беременных женщин.
Выявление в сыворотке присутствия одновременно IgG- и IgM-антител к инфекционному агенту можно трактовать как свидетельство недавнего первичного инфицирования, поскольку, как известно, срок исчезновения IgM-антител обычно составляет около 3 месяцев от начала инфекционного процесса. Но период циркуляции IgM антител может значительно варьировать в зависимости от инфекционного возбудителя и индивидуальных особенностей иммунного ответа организма. При инфицировании Toxoplasma gondii следовые количества IgM-антител к этим инфекционным агентам в некоторых случаях выявляются в течение 1-2 и более лет.
Таким образом, их присутствие в крови беременной женщины не всегда является подтверждением первичного инфицирования в период беременности. Кроме того, специфичность даже лучших коммерческих тест-систем для обнаружения IgM-антител не абсолютна. В некоторых ситуациях, как следствие очень высокой чувствительности тестов, возможны неспецифические ложноположительные результаты. Выявление в крови высокоавидных IgG антител в этой ситуации позволяет исключить недавнее первичное инфицирование. Низкоавидные IgG-антитела, в среднем, выявляются в течение 3-5 месяцев от начала инфекции (это может в определенной степени зависеть от метода определения), но иногда вырабатываются и в течение более длительного срока. Само по себе выявление низкоавидных IgG-антител не является безусловным подтверждением факта свежего инфицирования, но служит дополнительным подтверждающим свидетельством в ряду остальных серологических тестов. При реактивации инфекции выявляются специфические IgG высокой авидности.
Лечение
Большинство случаев приобретённой инфекции у иммунокомпетентных лиц разрешаются без специфической терапии. При хореоретините или поражении жизненно важных органов назначают комбинацию пириметамина с сульфадиазином. Альтернативой может быть комбинация пириметамина с клиндамицином при плохой переносимости сульфадиазина. При лечении хореоретинита и поражений ЦНС применяют глюкокортикоиды. ВИЧ-инфицированные пациенты с энцефалитом должны получать пожизненную супрессивную терапию для предотвращения рецидива инфекции.
При выраженной и бессимптомной врождённой инфекции в качестве начальной терапии рекомендуется комбинация пириметамина с сульфадиазином и фолиевой кислотой. Терапия, как правило, длительная, порой до 1 года. Лечение токсоплазмоза, возникшего во время беременности, в том числе и у ВИЧ-инфицированных женщин, следует проводить спирамицином. При заражении женщины в третьем триместре или инфицировании плода после 17 недель гестации используется комбинация пириметамина с сульфадиазином.
Показана высокая активность телитромицина in vitro в отношении Т.gondii (M. Kilinc, M. Hokelek, M. Erturk).
В исследованиях на животных показано, что atovaquone в сочетании с pyrrolidin dithiocarbamate вызывают конверсию тахизоитов в стадию тканевых цист (O. Djurkovic-Djakovic, A. Nikolic, B. Bobic, I. Klun).
Профилактика
Беременные женщины, чей серостатус не известен, или серонагативные должны избегать контакта с землёй и другими объектами, которые могут быть загрязнены фекалиями кошек, или работать в перчатках и мыть руки после работы. Домашние кошки, во избежание инфицирования, не должны питаться сырым мясом и пойманными грызунами. Необходимо проводить достаточную тепловую обработку мяса, мыть овощи и фрукты, мыть руки и кухонные поверхности после контакта с сырым мясом, овощами и фруктами.
Показания для назначения
1. Скрининговое обследование до и во время беременности.2. Лимфаденопатия во время беременности, если иммунитет к токсоплазме ранее отсутствовал или не исследовался.3. Признаки внутриутробной инфекции, фето-плацентарная недостаточность.4. Энцефалит/менингоэнцефалит при ВИЧ-инфекции, неопластических заболеваниях, приёме цитостатических препаратов, других иммунодефицитных состояниях.5. Лимфаденопатия неясной природы6. Гепатоспленомегалия неясной природы.7. Лихорадка неясной природы.8. Подозрение на врождённый токсоплазмоз.
Причины токсоплазмоза
Одноклеточный паразит, который является возбудителем токсоплазмоза, проникает в организм не только человека, но и различных животных, птиц, которые считаются промежуточными хозяевами. Чтобы пройти полный цикл развития, а главное размножиться, паразиту необходим кишечник кошки, поэтому любой зараженный представитель семейства кошачьих является его основным хозяином. Инфекция в стадии ооцисты вместе с фекалиями попадает в окружающую среду и долгое время сохраняет свою активность (1-2 месяца). Нужно сказать, что кошки выделяют ооцисты раз в жизни и обычно в возрасте котят. Следовательно, для человека возможные такие пути заражения:
- из окружающей среды — непосредственно от больной кошки (при контакте с ее слюной и кровью, если на коже есть царапины или ссадины, при уборке лотка), а также при работе с землей, которая может оказаться зараженной ооцистами;
- употребление в пищу зараженных продуктов (мясо животных, неправильно или плохо подвергшееся термической обработке, сырые яйца и молоко, грязные овощи, фрукты);
- во время беременности мать может инфицировать плод;
- в единичных случаях инфицирование возможно во время трансплантологических операций.
Токсоплазма, проникая в различные ткани человека, где в спящей форме в виде цист (латентная инфекция) может находиться на протяжении всей жизни. Здоровая иммунная система реагирует на это практически без симптомов или признаками легкой простуды. А вот при снижении иммунитета возникает обострение инфекции. Микроорганизмы с потоком крови разносятся по внутренним органам, поражают нервы, мышцы, сердце. Эта болезнь может иметь острую, хроническую и бессимптомную формы, быть приобретенной или врожденной. Группы риска — люди со слабой иммунной системой и беременные женщины.
Токсоплазмоз (количественный метод)
Токсоплазмоз (количественный метод)
Хроническое паразитарное заболевание, вызывающее, у лиц со сниженным иммунитетом, поражение нервной системы, сердца и других органов. Возбудитель – токсоплазмы. Источник инфекции – кошки и некоторые дикие представители семейства кошачьих. Путь передачи алиментарный. Серологические исследования на антитоксоплазменные IgG могут указывать на токсоплазмоносительство (при низких титрах) или на острую инфекцию (при высоких титрах). Определение токсоплазменных IgM используется для выявления врожденного токсоплазмоза или свежей инфекции (у детей и взрослых). Диагностическое значение имеет нарастание титра специфических антител в 4 и более раза. Если концентрация Toxo IgG в анализируемом образце 10 МЕ/мл и ниже, результат оценивают как отрицательный. Если концентрация Toxo IgG 40 МЕ/мл и выше, результат оценивают как положительный. В случае положительного результата ИФА на Toxo IgG у беременных важно определить срок инфицирования (исключить острый токсоплазмоз).
Microplate washer. Stat Fax 2600 Промывочный автомат для ИФА. Предназначен для промывки 96-луночных планшетов, используемых в ИФА (ELISA или EIA), включая клинические диагностические анализы, требующие промывки планшетов. Производства фирмы AWARENESS TECHNOLOGY INC, США
Для этого сыворотку анализируют на содержание Toxo IgМ, определяют индекс авидности Toxo IgG и исследуют динамику развития иммунного ответа.
Для уточнения диагноза НЕОБХОДИМО сдать:
— общий анализ крови; — на выявление антител (IgG, IgМ) к Toxoplasma gondii в плазме или в сыворотке крови методом ИФА; При отрицательном результате на Toxo IgМ и индексе авидности Toxo IgG более 50%, беременные в дальнейшем без клинических показаний в обследовании на токсоплазмоз не нуждаются. При положительном результате на Toxo IgМ сыворотку крови пациента оставляют в замороженном виде. Через 10-15 дней повторно делают забор крови и проводят анализ на Toxo IgG обоих образцов крови в сравнении. Увеличение концентрации Toxo IgG в динамике в 1,5 раза и более свидетельствует об инфицировании Toxoplasma gondii в пределах предыдущих 2 – 3 месяцев. Присутствие низкоавидных Toxo IgG подтверждает недавнее инфицирование. При концентрации Toxo IgG от 10 – 40 МЕ/мл результат считают промежуточным. Промежуточный результат может также свидетельствовать о начале развития иммунного ответа при острой стадии заболевания. Поэтому сыворотки с промежуточным результатом по Toxo IgG необходимо исследовать как потенциально положительные – в динамике на Toxo IgG и IgМ. — НЕЗАМЕДЛИТЕЛЬНО ОБРАТИТЕСЬ К ВРАЧУ. — после лечения, обязательно, сдать контрольные анализы, в том объеме, в котором проводилась диагностика заболевания.
Подготовка к исследованию
Требования к пробам: Для кошек: — мазок из прямой кишки (в пробирку Эппендорф с 0,5 мл физ. раствора)+венозная кровь в пробирке с ЭДТА (не менее 1 мл) или плазма (не менее 300 мкл) — для случаев, когда кошка сама становится промежуточным хозяином и проявляет соотвествующую симптоматику — кровь с ЭДТА, мин.объем — не менее 2 мл — при проявлении неврологической симптоматики, мазок со слизистых оболочек глаз + кровь с ЭДТА Для собак: — мазок со слизистых оболочек глаз + кровь с ЭДТА — кровь с гепарином не подходит для исследований методом ПЦР! КАТЕГОРИЧЕСКИ запрещено: оставлять ватные зонды в пробирке для смывов при предоставлении проб в лабораторию Хранение проб до доставки в лабораторию: — до 48 часов при +2-+8⁰С
Сдать анализ крови на токсоплазмоз
Токсоплазмоз — паразитарное инфекционное антропозоонозное заболевание, вызываемое Toxoplasma gondii. Токсоплазма имеет длительный цикл развития, основные этапы которого протекают в организме животных, птиц или человека. Также частицы токсоплазмы устойчивы к действую факторов внешней среды, поэтому могут длительное время сохраняться в испражнениях, земле, песке. Основной путь заражения — фекально-оральный и трансплацентарный. Так как конечным хозяином паразитов являются животные, чаще кошки, то особенное внимание уделяют контакту с ними. В свою очередь риск заражения кошек увеличивается при их контакте с грызунами. В окружающую среду токсоплазмы выделяются с испражнениями кошек, что способствует заражению человека при контакте с животным, либо местом, загрязненным частицами фекалий семейства кошачьих.
Попадание в организм человека обычно остается незаметным. Чаще всего заболевание протекает без выраженной клинической картины, либо возможны катаральные явления, симптомы интоксикации, что чаще отмечается у людей со сниженным иммунитетом.
Длительное время человек может являться носителем токсоплазмы и не догадываться об этом. Обычно факт подтверждается при проведении лабораторной диагностики. Так как особое значение носительство токсоплазмы имеет во время беременности, крайне важно уже в период планирования проходить скрининговое обследование, которое отражает наличие антител различных классов к токсоплазме. Это необходимо для исключения возможности инфицирования плода, ведь наибольшую опасность токсоплазма представляет для внутриутробное развития малыша. Именно во время беременности она может вызывать необратимые изменения в строении органов плода, приводя к порокам и потери беременности. Такая опасность появляется лишь при первичном инфицировании. Поэтому диагностика токсоплазмоза должна проводится как до беременности, так и во время нее, на сроке до 12 недель.
В комплекс обследования входит определение антител класса М и G к Toxoplasma gondii. В ответ на внедрение паразита организм начинает
вырабатывать антитела класса М, которые появляются в крови примерно через 2 недели, сохраняются до 8-10 недель. Через 8 недель от начала инфицирования начинают выделяться в кровь антитела класса G, которые принято считать антителами перенесенного заболевания. Наличие антител G без антител М говорит лишь о том, что организм ранее встречался с токсоплазмой, но в данный момент человек не болен, лечение не требуется. Эта информация крайне важна на этапе планирования беременности, во время беременности. Ведь наличие Ig G обеспечивает иммунитет к токсоплазме и исключает повторное инфицирование, которое крайне опасно во время беременности. Определение антител происходит методом ИХЛА, относящемуся к серологической диагностике и являющемуся объективным исследованием в комплексной диагностике токсоплазмоза.
Обычно определение антител класса G проводится комплексно с определением антител класса M, а также индекса авидности, что позволяет оценить давность заражения, стадию заболевания.
У новорожденных наличие антител класса G может говорить об их передачи от матери и не свидетельствуют о внутриутробном заражении.
Требование к биоматериалу
Прижизненная диагностика клинического токсоплазмоза базируется на следующей комбинации: 1. Четырехкратное или более повышение, понижение титра Ig G (в парных сыворотках, в течение 2-х недель) для острой стадии 2. Исключение других причин клинического синдрома 3. Ответ на химиотерапию Ранняя: продолжительность – до 1 года. Положительные Ig M, а к 3-ей неделе появляются и положительные Ig G специфические антитела (с пиком на 2-4 мес). Пик концентрации Ig M: конец первого, второй месяц, ПЦР по крови – положительная. Отрицательный результат только ПЦР исследования крови, ликвора – не исключает токсоплазмоз ни у клинически больного, ни у бессимптомного животного. Отрицательный результат на Ig G и ПЦР у клинически больного животного – доказывает отсутствие токсоплазмоза.Изменения в рутинных лабораторных исследованиях характерны больше для острого системного токсоплазмоза. Дополнительные исследования: ОАК: нерегенеративная анемия, эозинофилия, нейтрофилия, реже лимфо- моноцитоз. В тяжелых случаях у кошек – лейкопения со сдвигом влево. Биохимия крови: изменения зависят от поврежденных систем. Ликвор: повышение уровня белка, плеоцитоз (мононуклеарный). Гипопротеинемия, гипоальбуминемия. Поздняя: через 1 год после начала заболевания. Положительные Ig G специфические антитела. ПЦР по крови – отрицательная. Котята: рожденные от кошки с хронической стадией токсоплазмоза имеют материнские Ig G в течение 8-12 недель после рождени