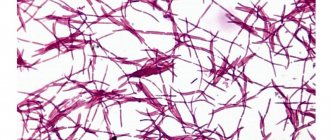
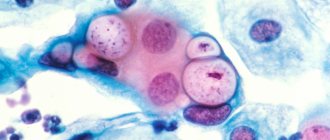
На коже и слизистых оболочках каждого человека обитает разнообразная кокковая флора. Гонококки, пневмококки и другие являются патогенными. Стрептококки и стафилококки, которые представляют большинство данной флоры, считаются условно-патогенными. Эти микроорганизмы присутствуют в небольших количествах и в своих обычных состояниях не вредны для микрофлоры человека. Однако из-за различных неблагоприятных факторов число стрептококков и других микроорганизмов стремительно растет и провоцирует воспалительный процесс.
Состав нормальной микрофлоры влагалища
Золотым стандартом диагностики в гинекологии является исследование мазка, взятого из заднего свода влагалища и цервикального канала. В норме могут быть обнаружены:
- 1Ацидофильные палочки Додерляйна (лактобактерии). В норме их количество должно составлять не менее 85-95% от всей флоры или 106-108 копий в образце.
- 2Бифидобактерии (около 10%).
- 3Пептострептококки, эубактерии, превотеллы, бактероиды, фузобактерии и другие анаэробные бактерии (5%).
- 4Другие кокки и грибы (в малом количестве).
- 5Эпителий (немного, его количество зависит от фазы менструального цикла).
- 6Лейкоциты (до 10 клеток).
Такое соотношение микроорганизмов способно длительно поддерживать слабокислую среду, позволяет бороться с патогенными бактериями, обеспечивает естественное увлажнение и местный иммунитет. Состояние микрофлоры влагалища оценивается с помощью лабораторных методов и имеет свою условную классификацию.
Степени чистоты влагалища
Понятие о степенях чистоты было введено для того, чтобы своевременно выявить женщин из группы риска по воспалительным заболеваниям половых органов (вагинит, цервицит, эндометрит и так далее). Об этом подробнее можно прочитать в другой нашей статье (перейдите по внутренней ссылке). Их выделяют на основании результатов простого мазка на флору и GN:
- 1Первая степень (второе название — нормоценоз): кислая среда. Нормальное количество лактобактерий, немного клеток эпителия, кокки отсутствуют. Встречается редко, как правило, наблюдается сразу после лечения, применения антибиотиков.
- 2Вторая степень: кислая среда. Число лактобактерий несколько снижено, появляются лейкоциты (до 10) и мелкие диплококки. Количество кокков незначительное (один или два плюса).
- 3Третья степень: среда становится слабокислой или щелочной. Количество палочек Додерляйна значительно ниже нормы, много эпителия, лейкоциты 10-30, кокковая или бациллярная флора преобладает, может обнаруживаться мицелий грибков. Это состояние и называют дисбиозом (дисбактериозом). Таким женщинам необходимо наблюдаться и вовремя получать лечение.
- 4Четвёртая степень: щелочная среда. Лактобациллы могут вовсе отсутствовать, большое количество клеток эпителия, лейкоцитов (выше нормы), много кокков или других патогенных бактерий. Эта степень соответствует вагиниту, следовательно, лечение женщины обязательно.
По мере сдвига pH в щелочную сторону меняется качество и количество флоры. Постепенно уменьшается уровень ацидофильных палочек, размножаются кокки, затем присоединяются грибы и другие бактерии.
Щелочная среда губительна для палочек Додерляйна, что приводит к развитию дисбактериоза влагалища.
Стоит отметить, что в нормальных мазках могут встречаться следующие микроорганизмы: гемолитический стрептококк, золотистый, эпидермальный и сапрофитный стафилококк, пептококки, микрококки, зелёный стрептококк и другие. Все они в небольшом количестве не представляют угрозы для здоровья и являются условно-патогенными представителями влагалищной флоры.
При 3-4 степени чистоты влагалища чаще всего можно обнаружить следующие виды кокков:
- 1Стрептококки. Как уже говорилось выше, эти микроорганизмы допускаются в небольшом количестве, но усиленное их размножение приводит к возникновению воспалительного процесса — вагиниту.
- 2Энтерококк фекальный. Часто встречается в кишечнике, при попадании в мочеполовые пути способен вызывать цистит или кольпит. Обнаружение его в мазках в большом количестве говорит о нарушении правил интимной гигиены, в том числе и во время секса.
- 3Стафилококк – условно-патогенный микроорганизм, в норме обитающий на коже. При усиленном его размножении способен вызвать серьёзное воспаление с поражением наружных и внутренних половых органов.
- 4Диплококк встречается при дисбиозе влагалища с нарушением нормального состава микрофлоры слизистой.
Существуют и другие кокки, они обычно вызывают неспецифические кольпиты.
Важно! Если в гинекологическом мазке выявлен золотистый стафилококк, то есть вероятность его обнаружения и на слизистых верхних дыхательных путей (ротоглотка, полость носа).
Вагиниты, вызванные условно-патогенной микрофлорой: рекомендации для практикующих врачей
Сведения об авторе:
Пустотина Ольга Анатольевна, доктор медицинских наук, профессор кафедры акушерства, гинекологии и репродуктивной медицины ФПК МР РУДН Адрес: 117198 Москва, ул. Миклухо-Маклая д. 6, телефон 8, email Pustotina Olga Anatolievna, Doctor of Medicine, Professor of The department of Obstetrics, Gynecology and Reproductive Health, Peoples’ Friendship University of Russia. Address: 117198 Moscow, Mikluho-Maklaya str, 6. Phone 8(495)7873827
Нормальная микрофлора женских половых органов
Естественная микрофлора влагалища и наружных половых органов представлена широким спектром сапрофитных и условно-патогенных микроорганизмов (УПМ). Из влагалища здоровых женщин репродуктивного возраста выделяют стрептококки, стафилококки, пептострептококки, бифидобактерии, коринебакте- рии, энтерококки, кишечную палочку, клебсиеллы, протей, фузобактерии, гардне- реллы, атопобиум, микоплазмы, бактероиды, грибы рода СапсИс1а, превотеллы, виелонеллы и др. Но содержаться они в небольшом количестве, не превышающем для каждого 103-104 КОЕ в 1 мл выделений. Основными представителями вагинальной микрофлоры являются молочнокислые анаэробные бактерии, принадлежащие к семейству 1_ас1:оЬааШ, которые значительно доминируют над УПМ и составляют 107-109 КОЕ/мл [1-3].
Лактобактерии поддерживают постоянство состава экосистемы влагалища и играют важную роль в неспецифической защите организма от инфекционной агрессии. Покрывая слизистую оболочку влагалища и шейки матки, они вырабатывают факторы гуморальной иммунной защиты, препятствуя адгезии на ней других микроорганизмов. Кроме того, лактобактерии обладают антагонистическими свойствами к некоторым представителям кишечной флоры — кишечной палочке, протею, клебсиелле, предохраняя влагалище от контаминации ими. В процессе своей жизнедеятельности они расщепляют гликоген, содержащийся в слизистой оболочке влагалища с образованием молочной кислоты и перекиси водорода, создавая среду с низким уровнем кислотности (рН 3,5-4,5), неблагоприятную для размножения других микроорганизмов [1-3].
Таким образом, во влагалище здоровых женщин репродуктивного возраста общая численность бактерий составляет 105-106 КОЕ/мл выделений, 95% которых представлены лактобактериями и только 5% формируется представителями других видов аэробных и анаэробных УПМ.
Вагиниты, вызванные УПМ
Вагиниты бывают воспалительного и невоспалительного характера. Воспалительные вагиниты в зависимости от вида возбудителя разделяют на неспецифические и специфические. К специфическим относятся трихомонадный, хламидийный, гонококковый и грибковый вагинит (вагинальный кандидоз), при обнаружении любых других УПМ вагинит является неспецифическим. Невоспалительный вагинит называется бактериальным вагинозом. Бактериальный ваги- ноз, неспецифический вагинит и вагинальный кандидоз объединяют вагиниты, вызванные УПМ.
Бактериальный вагиноз — это невоспалительное заболевание (дисбактериоз) влагалища, характеризующееся резким снижением количества молочнокислых бактерий и чрезмерно высокой концентрацией облигатных и факультативных анаэробных УПМ. Содержание лактобактерий составляет менее 106 КОЕ/мл, и преобладают среди них атипичные формы непродуцирующие перекись водорода. В результате уменьшения концентрации перекиси водорода и молочной кислоты, повышается уровень рН влагалищного содержимого >4,5 и создаются условия для роста УПМ. В большом количестве обнаруживаются Gardnerella vaginalis и Atopobium vaginae в синергизме со строгими анаэробами: Prevotella, Bacteroides, Fusobacterium, Peptococcus, Peptostreptococcus, Mobilluncus и др. кроме того, чаще и в больших количествах выделяются аэробные микробы (Streptococcus, Staphilococcus, Escherichia coli, Proteus, Klebsiella и др.) и микоплазмы (Mycoplasma hominis, Ureaplasma urealiticum, Ureaplasma parvo). общая численность бактерий во влагалище значительно возрастает и достигает 108-1011 кое/мл [4-6].
Бактериальный вагиноз встречается у каждой второй женщины, предъявляющей жалобы на патологические выделения из половых путей. Его частота в 2 раза выше вагинального кандидоза и в 5-10 раз — чем хламидийного, трихомонадного и гонококкого вагинита вместе взятого [1-3].
Бактериальный вагиноз не относится к инфекциям, передаваемым половым путем (ИППП), но связан с сексуальной активностью женщины и может вызывать симптомы уретрита у мужчин. Происходящие во влагалищном биотопе изменения облегчают восходящее инфицирование ИППП: гонококками, хламидиями, трихо- монадами, ВИЧ-инфекцией и др. Кроме того, накапливаясь в большом количестве, УПМ проникают в полость матки, вызывая хроническую воспалительную реакцию, приводя к бесплодию, невынашиванию беременности и снижению эффективности программ ЭКО [7, 8].
Неспецифический вагинит — это воспалительное заболевание слизистой оболочки влагалища, сопровождаемое лейкореей и другими признаками воспаления. Для него также характерно уменьшение колоний лактобактерий и увеличение количества УПМ, преобладающими среди которых, в отличие от бактериального вагиноза, являются аэробные бактерии, такие как стафилококки, стрептококки и представители семейства Еп1:егоЬас1:епасеае (кишечная палочка, клебсиелла, протей) [1-3].
Вагинальный кандидоз-это воспаление слизистой оболочки влагалища, вызванное дрожжевыми грибами рода СапсНс1а, которое встречается у 5-10% женщин репродуктивного периода. Развитие кандидоза в основном расценивают как вторичную эндогенную инфекцию, резервуаром которой является желудочно-кишечный тракт. Основными причинами, способствующими проникновению грибов из аногенитальной области во влагалище и их интенсивному размножению, является прием антибиотиков, глюкокортикоидов, потребление пищи с большим количеством углеводов. Предрасполагающими к заболеванию факторами служат ожирение, сахарный диабет и нарушение правил личной гигиены [9-11].
Факторы риска вагинитов, вызванных УПМ
Устойчивость экосистемы влагалища определяется факторами эндогенного и экзогенного происхождения. К развитию дисбиотических процессов в вагинальном микроценозе наиболее часто приводят: стресс, лечение антибиотиками, гормональная терапия, эндокринные и аллергические заболевания, снижение иммунной защиты организма, хронические запоры, инфекция мочевых путей. Уменьшение доли лактобацилл и повышение рН в содержимом влагалища происходит при повреждениях эпителиального покрова в результате полового акта, трещин, расчесов, при чрезмерной гигиене наружных половых органов. Нередко женщины при появлении неприятного запаха из половых путей прибегают к спринцеванию. Спринцевание не имеет ни гигиенического, ни профилактического, ни лечебного эффекта, а усугубляет дис- биоз и является фактором риска воспалительных заболеваний органов малого таза. Нарушение экосистемы влагалища может возникать после полового акта вследствие действия спермы с высоким уровнем рН, при частой смене половых партнеров, во время аногенитальных контактов, при использовании некоторых спермицидов. Длительное маточное кровотечение, инородные тела во влагалище (тампоны, пессарии, швы при истмико-цервикальной недостаточности) нередко также сопровождаются патологическими выделениями из половых путей [4, 6, 7, 9].
Клиника и диагностика вагинитов, вызванных УПМ
В основе вагинитов, вызванных УПМ, лежит уменьшение колоний лактобактерий, в результате которого изменяется рН вагинальной среды с кислой на щелочную и создаются условия для разрастания УПМ и их адгезии на освобождающийся эпителий слизистой оболочки влагалища.
Все происходящие изменения вагинального биотопа объединяются диагностическими критериями Амселя: появление специфических белей из половых путей, увеличение рН вагинального отделяемого, «рыбный» запах и наличие «ключевых клеток», представляющих собой эпителиальные клетки, порытые сплошным слоем различных микроорганизмов. По последним данным, даже наличие двух критериев из четырех позволяет установить нарушение вагинального микробиоценоза [5].
Вышеперечисленным критериям в полной мере может соответствовать любой вагинит, вызванный УПМ. Для дифференциальной диагностики необходимо (и вполне достаточно) проводить микроскопическое исследование вагинального отделяемого [7,12-14]. Микроскопическая картина будет представлена большим количеством микрофлоры различной формы и размеров, располагающейся как свободно, так и на поверхности эпителия в виде так называемых «ключевых клеток». Отличием между бактериальным вагинозом и неспецифическим вагинитом является лейкоцитарная реакция со стороны слизистой влагалища, которая при дисбиозе отсутствует, а при вагините — значительная, в следствие чего в вагинальном мазке будут обнаруживаться полиморфноядерные лейкоциты (ПЯЛ) в количестве более 20 в п/зр. Это обусловлено преобладанием аэробных стафилококков и стрептококков в содержимом влагалища, для размножения которых характерна тканевая воспалительная реакция с миграцией в очаг воспаления большого количества ПЯЛ [1-3].
При вагинальном кандидозе в микроскопической картине обнаруживаются споры и мицелии грибов нередко в комбинации с признаками бактериального вагиноза и/или неспецифического вагинита. Но, в отличие от последних, канди- доз может возникать не только в условиях дефицита лактобактерий, но и при их достаточном количестве. Грибы рода СапсМс1а прекрасно размножаются в условиях кислой рН вагинального содержимого [1, 10]. В следствие этого для дифференци- ровки нарушений вагинального микробиоценоза простой рН-метрии выделений не всегда достаточно.
Кроме того, возбудители ИППП, такие как хламидии, трихомонады, гонококк и Мусор1а5та депйаПит, также могут колонизировать генитальный тракт, не нарушая нормальный рост лактобактерий и не изменяя рН влагалищного содержимого, в следствие чего до 90% случаев инфицирования ИППП протекают бессимптомно. Поэтому международные и отечественные эксперты [12-15] рекомендуют дополнительно к микроскопическому исследованию, обладающему низкими диагностическими возможностями в отношении облигатных патогенов, использовать метод полимеразной цепной реакции (ПЦР) для выявления антигенов хламидий, трихо- монад, гонококка и Мусор1а5та депИаИит в отделяемом половых путей.
Таким образом, окончательный диагноз вагинитов, вызванных УПМ, устанавливается при наличии у женщины жалоб на патологические вагинальных выделения и данных микроскопического исследования, и только после исключения ИППП методом ПЦР.
Лечение вагинитов, вызванных УПМ
Первый этап: Противомикробная терапия.
Препаратами выбора для лечения бактериального вагиноза являются производные нитроимидазола и линкозамиды, которые наиболее активно подавляют размножение анаэробной микрофлоры:
- Метронидазол (2 г внутрь однократно, 500 мг 2 р/сут 5-7 дней, вагинальный гель 0,75% 5 г ежедневно 5 дней)
- Клиндамицин (300 мг 2 р/сут 7 дней, вагинальный крем 2% 5 г 7 дней, свечи 100 мг вагинально 3 дня)
- Тинидазол (2 г внутрь однократно) [12-15].
Исследования показали, что ни у одной из схем нет преимуществ в эффективности терапии [7], однако при местном использовании значительно реже возникают побочные эффекты [16].
Для лечения неспецифического вагинита рекомендуется использовать клин- дамицин (300 мг 2 р/сут 7 дней, вагинальный крем 2% 5г 7 дней, свечи 100 мг вагинально 3 дня). В сравнении с производными нитроимидазола (метронидазол, тинидазол, орнидазол), он имеет более широкий спектр действия, включающий не только анаэробные, но и аэробные грамположительные и грамотрицательные бактерии [3, 12, 13, 17, 18].
В последние годы опубликованы результаты крупных рандомизированных контролируемых исследований, показавших высокую эффективность лечения нарушений вагинального микробиоценоза еще двумя антибиотиками широкого спектра действия: рифаксимина (250 мг вагинально 5 сут) [19] и нифуратела (250 мг вагинально 10 сут) [20].
Следует отметить, что все выше представленные антибактериальные средства, обладая выраженной подавляющей активностью в отношении УПМ, не влияют на жизнедеятельность полезных молочно-кислых бактерий [15, 19, 20].
Терапия вагинального кандидоза проводится антимикотиками, среди которых препаратами первой линии являются азолы для интравагинального применения (имидазолы):
- Клотримазол крем 2% 5 гЗсут
- Миконазол крем 2% 5 г 7 сут, 4% 5 г 3 сут
- Миконазол свечи 100 мг 7 сут, 200 мг 3 сут, 1200 мг однократно
- Бутоконазол 2% 5 г 3 сут
- Тиоконазол 6,5% 5 г однократно
- Терконазол 0,4% 5 г 7 сут, 0,8% 5 г 3 сут
- Сертаконазол свечи 300 мг однократно;
и азолы для приема внутрь (триазолы):
- флуконазол 150 мг однократно
- итраконазол 200 мг 2 р/сут 1 день
При остром неосложненном вагинальном кандидозе, вызванном СапсМс1а а1Ысап5, все препараты местного и системного действия одинаково эффективны.
В случаях рецидивирования процесса длительность и количество курсов увеличивается, при этом необходимо идентифицировать вид кандидозной инфекции и исключить возможные факторы риска [10,12-14].
Антисептики:
В настоящее время получено множество доказательств эффективности терапии вагинитов, вызванных УПМ, различными антисептическими средствами, такими как:
- деквалиния хлорид 1 вагинальная таблетка 10 мг на ночь б сут
- хлоргексидина гидрохлорид 1 свеча 16 мг вагинально 2 р/сут 5 сут
- повидон-йод 1 свеча 200 мг вагинально на ночь 7 сут [б, 18, 21,22, 24].
Все антисептики обладают широким неспецифическим спектром действия и подавляют рост аэробных и анаэробных микроорганизмов, а также грибов рода СапсМс1а, при этом не влияя на жизнедеятельность колонии лактобактерий [15].
Наибольшая доказательная база (уровень доказательности 1А) продемонстрирована для деквалиния хлорида (флуомизина). В крупномасштабных многоцентровых рандомизированных зарубежных [21 ] и отечественных исследованиях (БИОС-1/М) [18, 22, 24] с участием 321 и 640 пациенток, соответственно, деквалиния хлорид показал сопоставимую эффективность с действием клиндамицина при лечении вагинитов, вызванный УПМ, при значительно лучшей переносимости и меньшей частоте развития кандидоза. Кроме того, вагинальные таблетки деквалиния хлорида обладают хорошей всасываемостью и меньшей текучестью в сравнении с хлоргексидином, поэтому назначаются один раз в сутки, не вызывая аллергических и других побочных эффектов, характерных для повидон-йода, при этом более эффективно уменьшая количество «ключевых клеток» и ПЯЛ в вагинальном мазке [18, 22].
Второй этап: восстановление микробиоценоза
В настоящее время стало очевидным, что проведение только антимикробной терапии при вагинитах, вызванных УПМ, является не достаточно эффективным [18, 23]. Как показал последний систематический обзор [7], через месяц после лечения только в 65-85% случаев отмечается клиническое и лабораторное улучшение, а в остальных — патологические выделения из влагалища рецидивируют.
Одной из причин хронизации процесса являются бактериальные пленки, формирующие невосприимчивость микроорганизмов к действию антибактериальных и антисептических средств [23]. В результате уровень излеченности через 3 мес составляет 60-70% и еще ниже через 6 мес [6]. Значительное повышение эффективности терапии вагинитов происходит после проведения второго этапа, направленного на восстановление нормального микробиоценоза [22, 23, 25].
Наилучшие результаты продемонстрировало применение пробиотиков, содержащих живые лактобактерии. Они не только подавляют рост УПМ, ассоциированных с бактериальным вагинозом и неспецифическим вагинитом, за счет образования молочной кислоты, перекиси водорода и бактериоцинов, но и способны разрушать образованные ими биопленки, а также модулируют иммунный ответ и способствуют размножению колоний эндогенных лактобактерий [4, 12, 19, 24, 26, 27].
В качестве дополнительного фактора, улучшающего состояние вагинального микробиоценоза после антимикробной терапии, является применение вагинальных таблеток аскорбиновой кислоты. [28]. В то же время, применение исключительно пробиотиков и/или закисления вагинальной среды без предшествующей антимикробной терапии для лечения вагинитов, вызванных УПМ, недостаточно [7].
Лечение вагинитов, вызванных УПМ, у беременных
Нарушение вагинального микробиоценоза у беременных достоверно сопряжено с повышенным риском преждевременных родов, восходящего инфицирования плода и послеродовых гнойно-септических осложнений [1,8, 29-31 ].
Согласно зарубежным рекомендациям [12, 13] терапия бактериального вагино- за и неспецифического вагинита у беременных женщин не отличается от таковой у небеременных. Препаратом первой линии считается метронидазол для системного и местного применения. При осложненном течении беременности и высоком риске преждевременных родов более эффективным считается назначение клиндамицина, обладающего более широким спектром активности [32-35]. При этом терапию нарушений биоценоза влагалища необходимо проводить с самых ранних сроков беременности [36].
В отечественных рекомендациях [14] антибиотики из группы нитроимидазола и линкозамидов противопоказаны в первом триместре, их применение возможно только местно после 12 нед беременности. Поэтому препаратами выбора для беременных являются вагинальные антисептики широкого спектра действия. Среди антисептических средств только у деквалиния хлорида безопасность применения на любом сроке беременности и в период грудного вскармливания подтверждена в масштабных многоцентровых исследованиях [18, 21, 22, 24]. Беременным с вагинальным кандидозом показано местное применение азолов (клотримазол, миконазол, терканозол и др.) [12-14]. В случаях неэффективности терапии предусмотрено интравагинальное назначение полиенов (натамицин, нистатин) [13-15]. В дальнейшем для профилактики рецидивов вагинальных выделений беременным назначаются пробиотики и средства, подкисляющие вагинальную среду [28, 36].
В заключение хочется отметить, что вагинальный микробиоценоз напрямую связан с состоянием здоровья женщины. Любые нарушения гомеостаза могут сопровождаться патологическими выделениями из половых путей, которые нередко бывают кратковременными, и после нормализации общего состояния самостоятельно проходят. В случаях рецидивирования процесса основной задачей врача является не поиск и идентификация возможных возбудителей, которых при вагинитах, вызванных УПМ, как правило множество, а выяснение причин, приведших к длительному течению заболевания. Для постановки правильного диагноза достаточно простой микроскопии вагинального мазка и метода ПЦР для исключения строгих патогенов. При рецидивирующих патологических вагинальных выделениях необходим также тщательный сбор анамнеза для выявления всех возможных факторов риска, только после устранения которых достигается полноценное восстановление вагинального микробиоценоза.
Список использованной литературы
1. Гуртовой Б.Л., Кулаков В.И., Воропаева С.Д. Применение антибиотиков в акушерстве и гинекологии. – М.: Триада-Х, 2004. – 176с.
2. Sweet RL, Gibbs RS. Infectious diseases of the female genital tract. – 5th ed. Lippincott Williams Wilkins, 2009. 469p.
3. Petersen EE. Infections in Obstetrics and Gynecology. New York: Thiem, 2006. -260p
4. Радзинский В.Е. Бактериальный вагиноз. В кн. Шейка матки, влагалище, вульва. Физиология, патология, кольпоскопия, эстетическая коррекция: руководство для практикующих врачей / Под ред. С.И. Роговской, Е.В. Липовой. – М.: Издат журнала StatusPraesens, 2014. – С.249-280.
5. Mittal V, Jain A, Pradeep Y. Development of modified diagnostic criteria for bacterial vaginosis at peripheral health centres in developing countries/ J Infect Dev Ctries. 2012; 6(5): 373-377.
6. Verstraelen H, Verhelst R. Bacterial vaginosis: an update on diagnosis and treatment/ Expert Rev Anti Infect Ther. 2009;7:1109–1124.
7. Donders GG, Zodzika J, Rezeberga D. Treatment of bacterial vaginosis: what we have and what we miss/ Expert Opin Pharmacother. 2014;15(5): 645-657.
8. Leitich H, Bodner-Adler B, Brunbauer M. et al. Bacterial vaginosis as a risk factor for preterm delivery: a meta-analysis/ Am J Obstet Gynecol. 2003;189: 139–147.
9. Filler SG. Insights from human studies into the host defense against candidiasis/ Cytokine. 2012; 58(1): 129-132.
10. Байрамова Г.Р. Рецидивирующий вульвовагинальный кандидоз: автореф. дис. докт.мед.наук.– М., 2013.
11. Роговская С.И., Липова Е.В., Яковлева А.Б. Вульвовагинальные микозы. В кн. Шейка матки, влагалище, вульва. Физиология, патология, кольпоскопия, эстетическая коррекция: руководство для практикующих врачей / Под ред. С.И. Роговской, Е.В. Липовой. – М.: Изд-во журнала StatusPraesens, 2014. – С.281-308.
12. CDC. Sexually Transmitted Diseases Treatment Guidelines 2010. https://www.cdc.gov/std/treatment/2010/pid.htm
13. Sherrard J, Donders G, White D. European (IUSTI/WHO) Guideline on the management of vaginal discharge in women reproductive age. 2011.
14. Клинические рекомендации РОАГ. Акушерство и гинекология. – 4-е изд./ под ред. В.Н. Серова, Г.Т. Сухих. – М.: ГЭОТАР-Медиа, 2014. – 1024с.
15. Профилактика, диагностика и лечение инфекций, передаваемых половым путем: рук-во для дерматовенерологов, акушеров-гинекологов, урологов и семейных врачей. – М.:Институт здоровья семьи, 2008.
16. Mikamo H, Kawazoe K, Izumi K, et al. Comparative study on vaginal or oral treatment of bacterial vaginosis / Chemotherapy. 1997; 43:60-68.
17. Практическое руководство по антиинфекционной химиотерапии// Под ред. Л.С. Страчунского, Ю.А. Белоусова, С.Н. Козлова. – М., 2007. – 462с.
18. Подзолкова Н.М., Никитина Т.И. Сравнительная оценка различных схем лечения больных с бактериальным вагинозом и неспецифическим вульвовагинитом // Рос вестник акуш гинекол, 2012.- №4. – С.75-81.
19. Donders GG, Guaschino S, Peters K, et al. A multicenter, double-blind, randomized, placebocontroled study of rifaximin for the treatment of bacterial vaginosis/ Int J Gynaecol Obstet. 2013; 120:131-136.
20. Mendling W, Caserini M, Palmieri R. A randomized, controlled study to assess the eficacy and safety of nifuratel vaginal tablets on bacterial vaginosis/ Sex Transm Infect. 2013;9 01: A28.
21. Weissenbacher ER, Donders G, Unzeitig V. et al. Fluomizin Study Group. A comparison of dequalinium chloride vaginal tablets (Fluomizin®) and clindamycin vaginal cream in the treatment of bacterial vaginosis: a single-blind, randomized clinical trial of efficacy and safety. Gynecol Obstet Invest. 2012; 73: 8–15.
22. Подзолкова Н.М., Никитина Т.И. Новые возможности терапии рецидивирующих вульвовагинальных инфекций: анализ и обсуждение результатов многоцентрового исследования БИОС-2 // Акуш и гинекол, 2014. — №4. – С.68-74.
23. Swidsinski A, Verstraelen H, Loening-Baucke V. et al. Presence of a polymicrobial endometrial biofilm in patients with bacterial vaginosis/ PLoS One. 2013;8:e53997.
24. Радзинский В.Е., Ордиянц И.М., Четвертакова Э.С., Мисуно О.А. Двухэтапная терапия вагинальных инфекций// Акуш и гинекол, 2011. — №5. – С.90-93.
25. McMillan A, et al. Disruption of urogenital biofilms by lactobacilli / Colloids Surf B Biointerfase,2011; 86(1): 58-64.
26. Larsson PG, Stray-Pedersen B, Ryttig KR, Larsen S. Human lactobacilli as supplementation of clindamycin to patients with bacterial vaginosis reduce the recurrence rate; a 6-month, double-blind, randomized, placebo-controlled study./ BMC Women Health, 2008;15(8):3.
27. Ya W, Reifer C, Miller L E. Efficacy of vaginal probiotic capsules for recurrent bacterial vaginosis: a double blind, randomized, placebo-controlled study. Am J Obstet Gynecol. 2010; 203:1200–1208.
28. Zodzika J, Rezerberga D, Donders G. et al. Impact of vaginal ascorbic acid on abnormal vaginal microflora / Arch Gynecol Obstet 2013; 288: 1039-1044.
29. Bothuyne-Queste E, et al. Is the bacterial vaginosis risk factor of prematurity? Study of a cohort of 1336 patients in the hospital of Arras/ J Gynecol Obstet Biol Reprod. 2012; 41(3): 262-270.
30. Pustotina OA, Bubnova NI, Yezhova LS. Pathogenesis of hydramnios and oligohydramnios in placental infection and neonatal prognosis /J mat-fetal&neonat med. 2008; 21(1): 267-271.
31. Pustotina OA. Urogenital infection in pregnant women: clinical signs and outcome /J Perinat Med, 2013; 41:135.
32. Simcox R, Sin WT, Seed PT, et al. Prophylactic antibiotics for the prevention of preterm birth in women at rick: a meta-analysis/ Aust N-Z J Obstet Gynaecol. 2007; 47: 368-377.
33. McDonald HM, Brocklehurst P, Gordon A. Antibiotics for treating bacterial vaginosis in pregnancy/Cochr Database Syst Rev. 2007. N1.P.CD000262.
34. Lamont RF, Duncan SLB, Mandal D, et al. Intravaginal clindamycin to reduce preterm birth in women with abnormal genital tract flora/ Obstet Gynecol. 2003;101:516–522.
35. Brocklehurst P, Gordon A, Heatly E, et al. Antibiotics for treating bacterial vaginosis in pregnancy/Cochr Database Syst Rev. 2013. N1.P.CD000262
36. Othman M, Neilson JP, Alfirevic Z. Probiotics for preventing preterm labor/ Cochr Database Syst Rev. 2007. N1.P.CD005941.
Причины появления кокков в гинекологическом мазке
Кокковая флора в мазке у женщин может наблюдаться по нескольким причинам:
- Несоблюдение женщиной правил личной гигиены. Сюда можно отнести неправильный и нерегулярный уход за половыми органами, редкая смена нижнего белья, постоянное использование ежедневных прокладок, применение щелочного мыла.
- Длительное бесконтрольное употребление антибиотиков.
- Частая смена половых партнёров, отказ от барьерных методов контрацепции, неправильное чередование анального, орального и вагинального секса в пределах одного полового акта, несоблюдение правил гигиены секса.
- Злоупотребление спринцеваниями, особенно с антисептиками (вымывание нормальной микрофлоры).
- Начало сексуальной жизни до 15 лет, отсутствие грамотности в плане интимной гигиены.
- Гормональные изменения у женщин в период менопаузы, при беременности, нарушениях менструального цикла.
- Общие соматические заболевания, хронические инфекции, прием глюкокортикоидов, которые ослабляют иммунитет.
- Механическое повреждение слизистой оболочки (нарушение естественной барьерной функции).
Какие симптомы могут наблюдаться?
Активное размножение кокковой флоры рано или поздно приведёт к появлению клинических симптомов заболевания. Признаки воспалительного процесса во влагалище неспецифичны, то есть по ним нельзя определить, какие именно кокки размножаются в половых путях.
Изменение состава микрофлоры женщина может заподозрить по следующим симптомам:
- Зуд, раздражение, жжение половых путей — эти симптомы могут отсутствовать.
- Изменение характера выделений из влагалища (жёлтые, белые, серые или зеленоватые, обильные, густые).
- Болевые ощущения или дискомфорт во время полового акта и в нижних отделах живота.
- Неприятный и резкий запах, но может и отсутствовать.
Симптомы кольпита достаточно яркие, не заметить их невозможно. Если игнорировать признаки заболевания, то инфекция может привести к следующим осложнениям:
- 1Неспецифический цервицит (воспаление слизистой оболочки шейки матки).
- 2Эндометрит, сальпингоофорит (появляются при снижении местного или общего иммунитета).
- 3Цистит, пиелонефрит часто развиваются на фоне вульвовагинита, имеют хроническое течение с частыми рецидивами. Они связаны с половым актом, при котором происходит занос флоры из половых путей в уретру.
- 4Присоединение патогенной флоры (трихомонады, грибы Кандида, хламидии). Нарушение микрофлоры способствует заражению ИППП при наличии инфицированного полового партнера.
- 5Осложнения нормальной беременности.
Micrococcus (микрококки, род бактерий)
Микрококки
(
Micrococcus
) — род грамположительных бактерий. Имеют форму сферы от 0,5 до 3 мкм в диаметре. Микрококки неподвижны. В природе распространены повсеместно: в почве, пыли, в воде. Особенностью микрококков является способность к развитию при низких температурах.
Micrococcus antarcticus
приспособлены к существованию в антарктических условиях. Отличается тем, что оптимальная температура роста 16±8°С, а могут расти и при 0°С (для сравнения, оптимальная температура роста для
Micrococcus luteus
и
Micrococcus lylae
— 37°С).
Микрококки в организме человека
Большое количество микрококков обитает на коже человек, они также встречаются в дыхательных путях, в ротовой полости. Чаще всего микрококки не вызывают каких-либо заболеваний, однако они могут быть причиной оппортунистических инфекций, особенно у индивидуумов с ослабленным иммунитетом, например, у ВИЧ-инфицированных.
В исследовании, проведённом в Твери, Micrococcus spp
. выделены из слизистой оболочки тела желудка у 22% здоровых детей (Апенченко Ю.С. и др.)
Микрококки в систематике бактерий
По современной классификации род Micrococcus
входит в семейство
Micrococcaceae
, порядок
Micrococcales
, класс
Actinobacteria
, тип
Actinobacteria
, царство Бактерии. В род микрококки включены виды:
Micrococcus aerogenes, Micrococcus alkanovora, Micrococcus aloeverae, Micrococcus antarcticus, Micrococcus chenggongense, Micrococcus cohnii, Micrococcus endophyticus, Micrococcus flavus, Micrococcus indicus, Micrococcus leteus, Micrococcus luteus, Micrococcus lylae, Micrococcus terreus, Micrococcus thailandicus, Micrococcus xinjiangensis, Micrococcus yunnanensis
.
Некоторые ранее входившие в состав данного рода бактерии реклассифицированы и в настоящее время относятся к другим родам (семействам) и имеют иные названия: Micrococcus agilis
(старое название)
—> Arthrobacter agilis
(новое);
Micrococcus halobius —> Nesterenkonia halobia; Micrococcus kristinae —> Kocuria kristinae; Micrococcus lactis —> Neomicrococcus lactis; Micrococcus mucilaginosus —> Rothia mucilaginosa; Micrococcus nishinomiyaensis —> Dermacoccus nishinomiyaensis; Micrococcus roseus —> Kocuria rosea; Micrococcus sedentarius —> Kytococcus sedentarius; Micrococcus varians —> Kocuria varians
.
На сайте GastroScan.ru в разделе «Литература» имеется подраздел «Микрофлора, микробиоценоз, дисбиоз (дисбактериоз)», содержащий статьи, затрагивающие проблемы микробиоценоза и дисбиоза отделов ЖКТ человека. Назад в раздел
Мазки во время беременности
В последнее время число воспалительных заболеваний и дисбиоза половых органов у беременных женщин увеличивается.
Это может быть связано с бесконтрольным приемом некоторых антибиотиков, гормонов (контрацепция перед планированием или для лечения бесплодия), неправильным питанием, образом жизни, снижением иммунитета. Появление кокковой флоры в мазках у беременных резко повышает вероятность присоединения патогенной флоры, чему способствуют:
- Изменение гормонального фона.
- Ослабление местного иммунитета на фоне вынашивания ребёнка.
Кроме того, многие препараты не рекомендованы для лечения беременных женщин, поэтому при появлении избыточной коккобациллярной микрофлоры возможности терапии значительно снижаются.
Активное размножение условно-патогенных бактерий влечёт за собой развитие воспаления слизистой влагалища, шейки матки, мочевого пузыря. Опасность их заключается в повышении риска внутриутробной инфекции с задержкой развития плода, невынашивания и других осложнений.
Кокковая флора
В мазке могут обнаруживаться диплококки, сарцины, стрептококки, стафилококки, энтерококки. Единичные кокки считаются вариантом нормы, но большое количество этих бактерий указывает на воспалительный процесс. Энтерококки, как и кишечная палочка, проникают в вагинальную среду из прямой кишки, и без лечения могут вызвать эндоцервицит – воспаление слизистой шейки матки.
Но самые неприятные представители кокковой флоры – гонококки, появляющиеся при заражении гонореей. Выявление даже единичных возбудителей требует срочного лечения. Женщины часто являются носителями гонококка, но при этом сами не испытывают симптомов половой инфекции. Не зная о своей болезни, они заражают партнеров, у которых возникает гонорейный уретрит.
В этом случае женщине показано антибактериальное лечение и обследование на других возбудителей ЗППП. Чаще всего для этого проводится ПЦР-реакция, обнаруживающая минимальное количество патогенных микробов и простейших.
Обнаружение кокковой флоры – плохой знак, указывающий на инфекционные воспалительные процессы, требующие лечения и повторного контроля после антибиотикотерапии.
Методы диагностики
Выявление кокков во влагалище у женщин возможно с помощью трех лабораторных анализов: простого мазка на флору, теста «Фемофлор» в модификации Фемофлор 8 (10) или Фемофлор 16 (17) и бакпосева.
Чаще всего у женщин используется простой мазок. Забор материала для исследования проводится из 2 или 3 точек: слизистая заднего свода влагалища, шейки матки и иногда уретры.
Перед взятием материала не следует спринцеваться, применять свечи с антисептиками, принимать антибиотики, заниматься сексом, так как результат будет искажён.
Биоматериал наносится на стерильные стёкла и изучается под микроскопом. При необходимости делается посев на питательные среды с определением чувствительности к антибиотикам.
Иногда исследования лишь мазков на флору бывает недостаточно для постановки диагноза, поэтому прибегают к дополнительным обследованиям (Фемофлор, ПЦР в режиме реального времени, УЗИ, PAP-тест, кольпоскопия и др.).
Дополнительная диагностика
При появлении симптомов нарушения функции половой системы (зуд и жжение во влагалище, обильные выделения темного окраса со специфическим запахом, боли в нижней части живота) важно незамедлительно обратиться к гинекологу для осмотра и лечения заболевания.Первым делом проверяется микрофлора женщины, делается три контрольных мазка:
- свод влагалища;
- канал шейки матки;
- уретра.
Образцы наносятся на специальное стекло и отправляются в лабораторию. Палочки кокковой и бациллярной флоры тщательно изучены, а потому не будет проблем с их идентификацией.При выявлении коккобациллярной флоры для дополнительных исследований может понадобиться кровь и моча. Только после проведения комплексного исследования удастся определиться с разновидностями кокков и бацилл, населяющих слизистую влагалища, а также установить их количество и наличие сопутствующих болезней.
Препараты для лечения
Лечение зависит от характера выявленной микрофлоры, симптомов заболевания и общего состояния женщины. При обнаружении большого количества кокков и лейкоцитов в мазке показана местная терапия в виде вагинальных свечей, овулей и капсул:
- 1Гексикон (хлоргексидин в виде свечей).
- 2Флуомизин (деквалиния хлорид).
- 3Тержинан, Полижинакс.
- 4Клиндамицин.
- 5Макмирор (нифурантел).
- 6Нео-Пенотран.
- 7Бетадин (сейчас используется все реже, часто вызывает неприятные ощущения, зуд, жжение).
- 8Местные антисептики в растворах — Мирамистин, Хлоргексидин.
При тяжелом воспалительном процессе назначаются системные антибиотики: цефтриаксон, цефиксим, амоксиклав и др.
Дополнительно могут быть назначены средства для восстановления нормальной вагинальной микрофлоры. Полноценных исследований по их применению не проводилось, однако этот вопрос активно изучается. Пробиотики не показаны при молочнице, так как могут спровоцировать ее рецидив.
Местные пробиотики в виде вагинальных свечей или таблеток:
- 1Вагинорм-С с аскорбиновой кислотой закисляет среду влагалища и нормализует состав микрофлоры, используют по 1 таблетке вагинально перед сном 6 дней.
- 2Ацилакт с живыми ацидофильными бактериями по 1 свече 2 раза за день 7-10 дней.
- 3Лактонорм по 1 вагинальной капсуле 2 раза в день 7 дней.
После лечения повторно берутся мазки для контроля эффективности терапии. При отсутствии эффекта назначаются альтернативные схемы или продлевается основной курс антибиотиков в виде вагинальных форм.
Лечиться можно амбулаторно, в домашних условиях. Из народных средств могут быть рекомендованы сидячие ванночки с ромашкой, календулой, раствором фурацилина.
Гели, кремы и спреи для восстановления микрофлоры влагалища
Восстановление микрофлоры влагалища
Кремы, гели и спреи относятся к категории местных гидрофильных средств. В отличие от более плотных, вязких и тяжелых мазей, имеющих жировую основу, эти средства намного легче наносить, они быстро впитываются, не оставляя ощущения жирной пленки.
Одно из эффективных средств, благотворно влияющих на вагинальную микрофлору – это восстанавливающий гель «Гинокомфорт®». Он не только помогает восстановить нормальную микрофлору, но и защищает от рецидивов заболевания в будущем. В состав средства входят такие натуральные компоненты, как масло чайного дерева, имеющее противомикробное и противовоспалительное действие, и экстракт ромашки, оказывающий регенерирующий эффект. Бисаболол и пантенол помогают справиться с раздражением и воспалительными процессами, а молочная кислота способствует восстановлению нормальной микрофлоры влагалища и поддержанию физиологического уровня кислотности.
Профилактика
Для предупреждения нарушений баланса микрофлоры половых путей нужно по возможности устранить все провоцирующие факторы:
- Устранить гормональный дисбаланс (ЗГТ при климаксе, оральные контрацептивы по показаниям).
- Соблюдать ежедневную интимную гигиену, а также во время менструации и секса. Отказаться от спринцеваний без назначения врача.
- Использовать презервативы.
- Вести здоровый образ жизни, быть активной, заниматься спортом или лечебной гимнастикой, правильно питаться, избегать частого употребления антибиотиков, беречь свой организм от инфекций.
- Одним из способов профилактики также является регулярное посещение гинеколога и лечение хронических заболеваний не только половой системы, но и других органов.