АсАТ и АЛТ
Тесты на АСТ и АЛТ – это два исследования, зачастую назначаемые врачом в комплексе. Почему уровень этих двух ферментов так важно определять одновременно? Впервые идею об информативности их соотношения выдвинул ученый Фернандо Де Ритис из Италии. Он использовал метод для дифференциальной диагностики гепатитов различных видов. С тех пор его имя стало нарицательным. Коэффициент Ритиса показывает соотношение активности АСТ и АЛТ. У здоровых людей коэффициент составляет 0,91-1,75. Показатель информативен только в том случае, если значения этих ферментов превышают референсные. Если в двойном тесте превышены только показатели АсАТ, это означает что поврежден миокард. При поражении сердечной мышцы уровень АСТ увеличивается в 8-10 раз, АЛТ – только в 1,5-2 раза. Если у пациента проблема с печенью, напротив, в 8-10 раз возрастает уровень АЛТ, а значения АСТ – лишь в 2-4 раза.
Показания к проведению анализа
Анализ на уровень АСТ назначает специалист в следующих случаях:
- Подозрение на патологии сердца;
- Мышечная дисфункция;
- Для определения состояния печени и ее дееспособности;
- Патологии почек;
- Болезни, появление которых спровоцировано инфекциями;
- Энцефалопатия непонятного происхождения;
- Аутоиммунные патологии;
- Желтуха и заболевания, связанные с нарушением выработки билирубина;
- Панкреатит в хронической форме;
- Гнойно-септические заболевания;
- Заболевания желчного пузыря;
- Болезни эндокринной системы;
- Онкологические патологии в злокачественной форме;
- Нетипичные реакции организма на воздействие аллергенов, в результате чего возникают заболевания эпидермиса;
- Травмы мышечной ткани;
- Подготовка к хирургическому вмешательству;
- В ходе проведения терапии для оценки эффективности лечения.
Анализ на АЛТ назначают в том случае, если существуют подозрения на патологии печени. При этом возникают следующая симптоматика:
- Болевой синдром в животе, локализующийся в области правого подреберья;
- Изменение цвета эпидермиса и белков глаз на желтый оттенок;
- Горечь в ротовой полости;
- Тошнота, сопровождаемая рвотой;
- Увеличение температуры тела;
- Ребенок быстро устает и плохо кушает.
Что представляет из себя фермент
АсАТ или АСТ – белок, синтезирующийся внутри клеток человеческого организма. Самые высокие его концентрации отмечаются в тканях миокарда, мышц и печени. В меньшей степени фермент присутствует в почках, поджелудочной железе, клетках центральной нервной системы и головном мозге. Кодируют его гены GOT 1 и GOT 2. У здорового человека уровень фермента достаточно низок. Его активный выброс в кровь начинается при разрыве сердечной мышцы, а также разрушении печени в результате гепатита, цирроза или онкологической опухоли. Фермент важен тем, что содержит в себе витамин B 6, задействованный в аминокислотном обмене и, соответственно, синтезе инсулина. В анализах показатель измеряется в единицах на литр крови.
Причины увеличения концентрации ферментов
Повышение АЛТ и АСТ у ребенка происходит в большинстве случаем, когда в организме развивается патологический процесс.
Увеличение концентрации АСТ происходит по следующим причинам:
- Закупорка желчных протоков;
- Заболевания крови;
- Патологии ревматологического характера;
- Онкологические патологии в злокачественной форме;
- Заболевания сердца;
- Воспаление, которое происходит в тканях мускулатуры;
- Интоксикация печени и патологии этого внутреннего органа;
- Плохое кровоснабжение печени;
- Заболевания ЖКТ;
- Генетическая патология, связанная с плохим метаболизмом меди;
- Заболевания щитовидной железы.
Концентрация АЛТ увеличивается в следующих ситуациях:
- Практически все формы гепатита;
- Патологии печени, в том числе наследственные;
- Отравление тяжелыми металлами;
- Онкологические заболевания печени злокачественного характера;
- Воспаление мягких мышечных тканей;
- Патологии сердца;
- Закупорка желчных протоков;
- Дистрофия мускулатуры.

Увеличение уровня АСТ и АЛТ также происходит и не из-за заболеваний. Причинами тому могут быть:
- Нарушение правил сдачи биоматериала на исследование;
- Послеоперационный период;
- Употребление некоторых медикаментозных препаратов.
Спектр применения анализа на АСТ
- В кардиологии в качестве маркера инфаркта миокарда. В сердечной мышце фермент активен более чем в 10 000 раз нежели в крови. При инфаркте происходит интенсивное выделение фермента.
- При патологиях печени. Такие заболевания как гепатит и цирроз непременно сопровождаются разрушением тканей печени и резким скачком значений АСТ.
- При хроническом алкоголизме.
- В акушерстве и гинекологии. Во время беременности у женщины может происходить незначительное повышение значений АсАТ. Это объясняется воздействием растущего плода на печень матери. В первом триместре его значения не должны превышать 31 Ед/л, во втором и третьем – 30 Ед/л.
- В эндокринологии при сахарном диабете и/или избыточном весе.
Нормы ферментов для детей
В каждой лаборатории установлены свои референсные значения этого фермента. Обычно ориентируются на две основные единицы измерения содержания белка в организме – мкат/л и Ед/л.
В связи с этим референсные значения белка у детей будет разными.

Таблица 1. Норма АСТ у детей в мкат/л
| Возраст | Норма, мкат/л |
| До 1 месяца | 0,38-1,21 |
| От 1 до 12 месяцев | 0,27-0,97 |
| От года до 16 лет | 0,10-0,63 |
Таблица 2. Норма АСТ у детей в Ед/л
| Возраст | Норма, Ед/л |
| До 1 месяца | До 73 |
| От 1 до 12 месяцев | До 58 |
| От года до 16 лет | До 38 |
Исходя из этих референсных значений, выполняют расшифровку анализа.
У АЛТ также существуют свои референсные значения.
Таблица 3. Норма АЛТ у детей
| Возраст | Норма, ед/л |
| До 12 месяцев | До 60 |
| От 1 года до 3 лет | 40-45 |
| От 3 до 6 лет | |
| От 6 до 12 лет |
Как подготовиться к анализу
Чтобы повысить степень достоверности анализа, следует соблюдать некоторые правила и ограничения. Так накануне исследования стоит воздержаться от употребления жирной и копченой пищи, а также кондитерских изделий. Лучше всего, если тест будет проведен на голодный желудок с утра. При приеме лекарственных препаратов нужно проконсультироваться с врачом насчет их возможной отмены. Дело в том, что при биохимическом анализе крови многие медикаменты могут воздействовать на результаты исследования. При лечении антидепрессантами, антибиотиками, мочегонными и другими препаратами, показания тест могут быть искажены. Кроме того, непосредственно перед визитом в процедурный запрещается выполнять УЗИ, рентгенологическое исследование и процедуры физиотерапии.
Как проводится исследование
Анализ проводится в лабораторных условиях. У детей старшего возраста биоматериал забирают из вены, младшего – из пятки. Для грудничков не установлено специальных правил сдачи анализа. Детям постарше рекомендуется придерживаться следующих рекомендаций:
- Биоматериал забирается в утренние часы на голодный желудок;
- До исследования ребенку следует обеспечить комфортные психологические условия и снизить физические нагрузки;
- За несколько дней до анализа из рациона убирают жирную, острую, копченую и соленую пищу;
- За несколько дней до сдачи биоматериала прекращают давать ребенку медикаментозные средства, а если прерывать терапию не представляется возможным, список лекарственных препаратов предъявляют врачу или специалисту, который будет проводить анализ.
Расшифровка анализа на АсАТ
Норма у женщин
Значения анализа на АсАТ различаются в зависимости от возраста и пола. Так у женщин норма фермента в крови составляет 31 Ед/л. Чем старше человек, тем ниже его активность в организме. Это связано с замедлением обмена веществ в целом. Такое естественное физиологическое состояние, как беременность, также оказывает влияние на уровень фермента. В этот период могут наблюдаться его небольшие скачки как в одну, так и в другую сторону.
Норма у мужчин
Концентрация фермента у мужчин начинает превышать его количество у женщин начиная с 12-17 лет. Более высокие его концентрации объясняются большим объемом мышечной ткани. В пубертатном возрасте норма АСТ у мальчиков около 29 Ед/л. Это примерно на четыре единицы выше, чем у девочек в том же возрасте. У взрослого мужчины уровень фермента может достигать 37 Ед/л.
Гепатопротекторная терапия при заболеваниях печени у детей
Неалкогольная жировая болезнь печени (НАЖБП) является актуальной проблемой современной педиатрии. Следует отметить, что в последние годы отмечается рост числа детей, страдающих НАЖБП. При этом в 23–53% случаев развитие НАЖБП у детей связано с избыточной массой тела или ожирением [1–3].
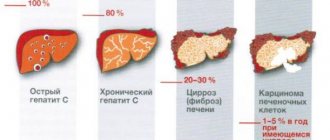
НАЖБП представлена двумя клиническими формами: жировая дистрофия печени (стеатогепатоз), неалкогольный стеатогепатит (НАСГ). Неалкогольный стеатогепатит — это хроническое заболевание печени с гистологическими признаками алкогольного гепатита у лиц, не употребляющих алкоголь в значимых гепатотоксических дозах [2–5].
Согласно современным представлениям выделяют первичную и вторичную НАЖБП. Первичная НАЖБП наиболее часто развивается при наличии сахарного диабета 2-го типа, ожирения и гиперлипидемии, может являться проявлением метаболического синдрома [6].
Причинами вторичного стеатоза печени и НАСГ у детей могут являться [7]:
- лекарственные препараты (глюкокортикоиды, синтетические эстрогены, противоопухолевые, антибактериальные, нестероидные противовоспалительные препараты и др.);
- синдром мальабсорбции вследствие хирургического вмешательства (как последствия наложения илеоеюнального анастомоза, билиарно-панкреатической стомы, расширенной резекции тонкой кишки и др.);
- хронические заболевания желудочно-кишечного тракта, сопровождающиеся синдромом мальабсорбции (хронический панкреатит, неспецифический язвенный колит);
- длительное (более 2 недель) парентеральное питание;
- быстрое снижение массы тела;
- абеталипопротеинемия, липодистрофия конечностей, болезнь Вебера–Крисчена, болезнь Вильсона–Коновалова;
- синдром избыточного бактериального роста.
Надо отметить, что при НАЖБП у детей в 48–100% случаев могут отсутствовать симптомы, характерные для патологии печени. При этом у 20–30% могут наблюдаться неопределенный дискомфорт, тяжесть, ноющие боли в правом подреберье, астенический синдром. Некоторые дети жалуются на отрыжку и изжогу, что чаще всего связано с ожирением. Гепатомегалия может выявляться в 75% случаев.
В крови обычно наблюдается повышение уровня аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ). При этом соотношение АСТ/АЛТ обычно ниже 1, а возрастание данного соотношения наблюдается при развитии фиброза печени. Кроме того, возможно незначительное повышение щелочной фосфатазы (ЩФ) и гаммаглутамилтрансферазы до двух норм, гипербилирубинемия до 1,5–2 норм и дислипидемия. Гипоальбуминемия и удлинение протромбинового времени могут свидетельствовать о развитии цирроза печени [5, 8, 9].
При ультразвуковом исследовании выявляется дистальное затухание эхосигнала, диффузная гиперэхогенность печени («яркая печень»), увеличение эхогенности печени по сравнению с почками и нечеткость сосудистого рисунка.
Проведение компьютерной томографии при НАЖБП позволяет выявить снижение рентгеноплотности печени до 3–5 ед (при норме 50–75 ед). При этом рентгеноплотность печени меньше рентгеноплотности селезенки. Визуализация внутрипеченочных сосудов, воротной и нижней полой вен как более плотных структур по сравнению с печеночной тканью. Для очаговой жировой дистрофии характерно пересечение нормальными кровеносными сосудами печени зон пониженной рентгеноконтрастности [8, 9].
К основным гистологическим признакам НАСГ относятся: 1) жировая дистрофия гепатоцитов (крупно- и мелкокапельная); 2) смешанная воспалительная инфильтрация (нейтрофилы, лимфоциты, макрофаги); 3) фиброз (преимущественно перивенулярный); 4) дополнительные (непостоянные) признаки — тельца Мэллори, фокальные центролобулярные некрозы, отложения железа [8, 9]. Прежде чем говорить о НАЖБП, необходимо провести комплексное обследование ребенка [5].
При подтверждении НАЖБП у ребенка важно подобрать эффективный и безопасный метод лечения для предотвращения прогрессирования заболевания и терапии уже имеющихся нарушений.
Основной целью терапии при НАЖБП является предотвращение прогрессирования болезни и развития цирроза. В настоящее время не существует единого стандарта лечения пациентов с НАЖБП. Основные направления терапии: коррекция ожирения и инсулинорезистентности; уменьшение перекисного окисления липидов и окислительного стресса (табл. 1).
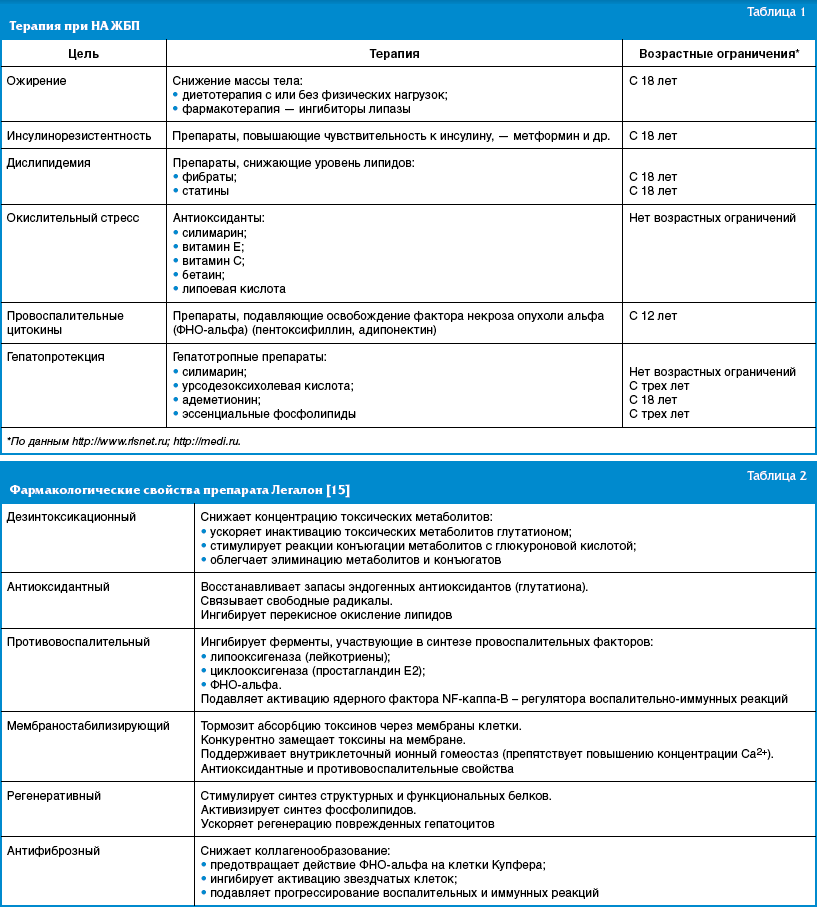
Наиболее важным при лечении НАЖБП является снижение массы тела. При этом не рекомендована резкая потеря веса, которая может способствовать усилению воспалительного процесса и образованию фиброза печени. Необходимо отметить, что часть препаратов, разрешенных для лечения взрослых пациентов, для применения в педиатрии не зарегистрирована, а некоторые разрешенные препараты не обладают достаточной эффективностью.
Так, например, в России орлистат не разрешен для применения у детей. Метформин, который в зарубежной практике применяется с 10-летнего возраста при метаболическом синдроме и сахарном диабете 2-го типа, не всегда эффективен. Согласно последним исследованиям, 6-месячный курс терапии данным препаратом улучшал метаболический профиль, но не оказывал влияния на гистологическую картину печени [5].
Достаточно эффективным препаратом, который применяется при НАЖБП, тормозит прогрессирование заболевания и обладает антифибротическим действием, является стандартизированный силимарин — Легалон. Легалон — лекарственное средство из растительного сырья. Активная субстанция выделена из плодов и млечного сока расторопши пятнистой (чертополох молочный). Расторопша в течение тысячелетий использовалась как лекарственное средство, и только в 1968 г. в Мюнхенском институте фармацевтики был расшифрован биохимический состав расторопши пятнистой. Главным составляющим компонентом лекарственного растения расторопша являются флавоноиды с гепатопротекторными свойствами: силибинин, силидианин, силикристин (общее название смеси этих соединений — силимарин). Экстракт силимарина водорастворим и плохо всасывается в кишечнике. Для повышения биодоступности активного вещества лекарственного препарата Легалон используется запатентованный процесс совместной преципитации, при котором биодоступность эталонного силимарина повышается до 85% (биодоступность других силимаринов не более 20%). Во всех странах действует международный патент на галеновую форму стандартизированного силимарина, увеличивающую всасывание активного вещества.
Доказано, что эффективность и безопасность силимарина зависит от соотношения флаволигнанов в лекарственном препарате и дозы силибинина. Отличие состава приводит к изменению в фармакинетике и, следовательно, клинической эффективности при лечении заболеваний печени различной этиологии.
Анализ силимаринсодержащих лекарственных препаратов (профиль высокоэффективной жидкостной хроматографии) установил, что по общему содержанию биологически активных веществ (флаволигнанов) первое место занимает Легалон, а последнее — Карсил, который содержит флавонолигнанов в 5 раз меньше, чем Легалон.
В составе препарата Легалон, по сравнению с другими препаратами, более высокое содержание силикристина и силибинина [15].
Силибинин является основным фармакологически активным веществом. Многочисленные экспериментальные и клинические исследования позволили уточнить механизм действия и клиническую эффективность силимарина при острых и хронических заболеваниях печени. В результате установлено, что эталонный силибинин (Легалон) обладает антифибротической, антиоксидантной, антитоксической, цитопротекторной, противовоспалительной, иммуномодулирующей, противоопухолевой активностью (табл. 2) [10, 11].
Легалон рекомендован для лечения токсических и лекарственных поражений печени.
В Западной Европе на острый лекарственный гепатит приходится 15–20% молниеносных гепатитов, в Японии — 10%, в России — 5%. В этиологическом плане на первом месте находятся противотуберкулезные и антибактериальные средства, затем нестероидные противовоспалительные препараты, лекарства, регулирующие функции нервной системы, гормональные, цитостатические, гипотензивные, антиаритмические препараты.
Патологический процесс начинается при действии гепатотоксикантов — стеатоз, некроз, холестаз, фиброз (цирроз). Лекарственное вещество при биотрансформации недостаточно теряет свою токсичность и/или в процессе метаболизма исходно нетоксичного соединения возникают промежуточные или конечные гепатотоксичные метаболиты. Болезнь возникает при передозировке лекарств, дефиците субстратов конъюгации, коферментов и ферментов, необходимых для детоксикации. При этом токсическое вещество может непосредственно воздействовать на структуру гепатоцита (например, токсический метаболит парацетамола — N-ацетил-р-бензохинон) и/или оказывать опосредованное влияние на специфические метаболические реакции (например, торможение синтеза белка при применении цитостатических антибиотиков). Классическим препаратом с облигатным гепатотоксическим действием является парацетамол. С другой стороны, поражение печени может быть вызвано генетически детерминированными особенностями метаболизма или повышенной восприимчивостью организма к лекарственному веществу, который не является гепатотоксикантом. Этот вид патологии не воспроизводится в эксперименте и не носит дозозависимый характер [12].
У детей наиболее часто наблюдаются поражения печени по типу острого гепатита (приблизительно в 80% случаев). Хроническое лекарственное поражение печени может быть самостоятельным заболеванием, но чаще развивается как исход острого гепатотоксического патологического процесса (при длительном поступлении лекарств). Тяжесть течения лекарственно-индуцированных заболеваний печени варьирует от бессимптомного повышения трансаминаз до развития фульминантной печеночной недостаточности. У детей чаще наблюдается бессимптомное повышение трансаминаз. Реже, при серьезных поражениях печени, может наблюдаться желтуха, кожный зуд, «печеночные знаки», кровоточивость, увеличение печени и болезненность при ее пальпации. При иммуноопосредованном поражении могут наблюдаться миалгии и артралгии, конъюнктивит, ринит, кожная сыпь, лимфаденопатия, лихорадка. Лекарственные поражения печени могут возникать уже через 48 часов на фоне приема препаратов. В некоторых случаях заболевание может проявиться через несколько недель или месяцев. Некоторые лекарственные реакции транзиторные и разрешаются самопроизвольно.
В зависимости от степени повышения уровней АЛТ и ЩФ острое повреждение печени классифицируют как гепатоцеллюлярное (цитолитическое), холестатическое или смешанное, сочетающее признаки холестаза и цитолиза (табл. 3).
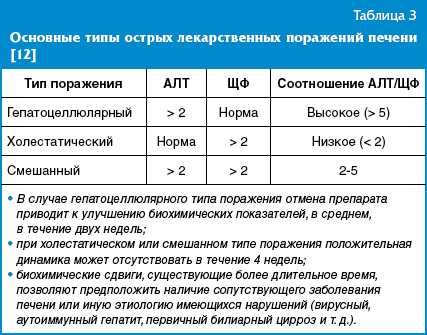
В детском возрасте чаще встречается гепатоцеллюлярный тип повреждения (в 2/3 случаях).
Повышение АЛТ является наиболее чувствительным тестом ранней диагностики лекарственного гепатита. При митохондриальных гепатоцитопатиях может повышаться и активность аспартатаминотрансферазы (АСТ). При коэффициенте де Ритиса (АСТ/АЛТ) меньше 1 повышение трансаминаз трактуется как воспалительный тип ответа, больше 1 — как некротический тип.
Особенностью холестатических форм лекарственного поражения печени является нередкое отсутствие гипертрансаминаземии. При этом развиваются желтуха и зуд кожи, но общее самочувствие, как правило, не страдает.
Обычно для профилактики и лечения лекарственного гепатита применяются гепатопротекторы. Учитывая механизмы действия, Легалон является препаратом выбора при лекарственном гепатите.
В педиатрии используется следующая схема подбора дозы Легалона: стандартизированный силимарин — 5 мг/кг/сут (3 раза в день с едой, водой). Детям до 40 кг — 70 мг/сут (1 капсула Легалона по 70 мг) в сутки; 41–60 кг — 240 мг/сут (2 капсулы Легалона по 70 мг в сут); 61–70 кг — 320 мг/сут (3 капсулы Легалона по 70 мг в сут) [14].
Клиническое наблюдение
В отделении гастроэнтерологии МНИИ педиатрии и детской хирургии наблюдались дети с НАЖБП — 9 детей (6 мальчиков и 3 девочки) в возрасте от 11 до 15 лет. При поступлении у 4 детей (44%) отмечались периодические боли в животе, у 3 (33%) — изжога, у 5 (56%) — отрыжка. Ожирение наблюдалось у 7 детей (78%). При этом средний индекс массы тела (ИМТ) в данной группе детей равнялся 97,5 ± 1,2 перцентиля.
Все дети были тщательно обследованы с целью уточнения характера поражения печени. В результате обследования у 7 детей был выявлен стеатогепатит, у двоих детей наблюдался стеатогепатоз на фоне гиперлипидемии. При этом у всех детей со стеатогепатитом наблюдалось повышение уровня АЛТ в крови (105 ± 19,5 Ед/л) и только у 5 (71%) наблюдалось повышение уровня АСТ (75,2 ± 11,4 Ед/л). У 4 (57%) детей наблюдалось повышение ЩФ и у 1 (14%) — повышение уровня гамма-глютамилтранспептидазы (ГГТП) в пределах 1,5 норм. Уровень общего билирубина был незначительно повышен у 3 детей (43%).
У одного ребенка со стеатогепатозом наблюдалось повышение уровня холестерина в крови, у второго — повышение холестерина и триглицеридов. При ультразвуковом исследовании у всех детей выявлялись признаки стеатоза — дистальное затухание эхосигнала, диффузная гиперэхогенность печени, нечеткость сосудистого рисунка. При этом у 5 (56%) из них была гепатомегалия.
Всем детям была назначена диетотерапия и Легалон в возрастной дозировке от 5 до 10 мг/кг/сут (1–3 капсулы в сут) на 1,5 месяца. В качестве критериев эффективности рассматривалась динамика клинических (улучшение общего состояния, уменьшение диспепсических расстройств, размеров печени), биохимических (нормализация уровней АЛТ, АСТ, ГГТП) и ультразвуковых (уменьшение размеров печени, улучшение эхоструктуры) показателей.
При обследовании пациентов через 1,5 месяца боли в животе сохранялись у 2 детей (22%), изжога — у 1 ребенка (11%), отрыжка — у 2 детей (22%). Масса тела несколько снизилась у 4 детей (57%) с ожирением, у 3 детей (43%) — масса тела не изменилась. При этом средний ИМТ в данной группе детей составил 96,6 ± 1,0 перцентиля. При исследовании биохимических показателей выявлялось достоверное снижение активности сывороточных трансаминаз (АЛТ — 51,1 ± 18,2 Ед/л, АСТ — 43,5 ± 6,6 Ед/л). При этом у 5 детей (56%) уровень АЛТ нормализовался, а у 2 (22%) снизился. Уровень АСТ нормализовался у 3 детей (33%) и у 2 (22%) — снизился. Уровень ГГТП после лечения был нормальным у всех детей. ЩФ снизилась до нормальных показателей у 2 детей, билирубин — у одного ребенка. У остальных детей данные показатели (ЩФ и билирубин) существенно не менялись.
Что касается детей с гиперлипидемией, у одного пациента после лечения нормализовался уровень холестерина, у второго — уровень триглицеридов.
Более того, на фоне лечения Легалоном наблюдалась положительная динамика ультразвуковой картины в виде уменьшения размеров печени у 3 детей из 5 (60%), а у 5 детей из 9 (56%) — выявлялось улучшение ее эхогенности.
Таким образом, Легалон является эффективным гепатопротекторным препаратом, который способствует достоверному уменьшению трансаминаз в крови и улучшению ультразвуковой картины печени у детей с НАЖБП.
В связи с выраженной положительной динамикой терапия, включающая диету и Легалон, была продолжена еще на 3 месяца с назначением последующего контрольного исследования крови и проведения УЗИ брюшной полости.
Также в нашем отделении наблюдались 4 детей с лекарственным гепатитом, трое из них получали длительную противосудорожную терапию и один ребенок получал парацетамол в течение трех дней, затем ему была назначена антибактериальная терапия на 10 дней. На фоне терапии у детей отмечалось бессимптомное повышение трансаминаз в крови. При этом у всех четверых наблюдалось повышение уровня АЛТ в крови (104,3 ± 14,1 Ед/л), у двоих — повышение АСТ (87,5 ± 11,5 Ед/л). Остальные показатели были в норме.
В связи с этим всем детям на фоне основного лечения был назначен Легалон в качестве гепатопротекторного средства в возрастной дозировке 5 мг/кг/сут.
У ребенка, получавшего парацетамол и антибактериальную терапию, повышение трансаминаз (АЛТ и АСТ) было обнаружено на второй день антибактериальной терапии (лекарственный гепатит мог быть связан и с приемом парацетамола, и с приемом антибактериальний терапии), и в тот же день была назначена гепатопротекторная терапия препаратом Легалон. Через 2 недели (через неделю после окончания приема антибиотика) при повторном исследовании биохимического анализа уровень трансаминаз в крови был в норме. Легалон способствовал более быстрому восстановлению функции печени.
Что касается детей, получавших противосудорожную терапию, то через месяц на фоне приема Легалона уровень трансаминаз полностью нормализовался. С профилактической целью данные дети продолжали получать Легалон на фоне противосудорожной терапии и после нормализации показателей.
Таким образом, стандартизированный силимарин (Легалон) является рациональным гепатопротекторным препаратом, который рекомендуют применять детям с различными заболеваниями печени с профилактической и с лечебной целью. Продолжительность терапии зависит от тяжести заболевания и проводится от месяца и более.
Литература
- Tominaga K., Kurata J. H., Chen Y. K. et al. Prevalence of fatty liver in Japanese children and relationship to obesity: an epidemiological ultrasonographic survey // Dig Dis Sci. 1995; 40: 2002–2009.
- Schwimmer J. B., Deutsch R. K., Kahen T. et al. Prevalence of fatty liver in children and adolescents//Pediatrics. 2006; 118: 1388–1393.
- Arslan N. B., Buyukgebiz B., Ozturk Y. et al. Fatty liver in obese children: prevalence and correlation with anthropometric measurements and hyperlipidemia // Turk J Pediatr. 2005; 47: 23–27.
- Paul Angulo. Nonalcoholic Fatty Liver Disease // N Engl J Med. 2002; 346: 1221–1231.
- Каганов Б. С. Детская гепатология. М.: Издательство «Династия», 2009. 576 с.
- Burt A. D., Mutton A., Day C. P. Diagnosis and interpretation of steatosis and steatohepatitis // Semin Disgn Pathol. 1998; 15: 246–258.
- Hassink S. G. A Clinical Guide to Pediatric Weight Management and Obesity. Lippincott Wiliams and Wilkins, 2007; 114–129.
- Pinto H. C., Baptista A., Camilo M. E., Valente A., Saragoca A., de Moura M. C. Nonalcoholic steatohepatitis: clinicopathological comparison with alcoholic hepatitis in ambulatory and hospitalized patients // Dig Dis Sci. 1996; 41: 172–179.
- Perrie E., Pardee B. S., Joel E. Lavine, Jeffrey B. Schwimmer. Diagnosis and Treatment of Pediatric Nonalcoholic Steatohepatitis and the Implications for Bariatric Surgery. Seminars in Pediatric Surgery. Volume 18, Issue 3, Pages 144–151, August 2009.
- Saller R., Meier R., Brignoli R. The use of silymarin in the treatment of liver diseases // Drugs. 2001; 61: 2035–2063.
- Буторова Л. И., Цибизова Т. А., Калинин А. В. Возможности использования Легалона при неалкогольной жировой болезни печени // Экспериментальная и клиническая гастроэнтерология. 2010. № 5. С. 69–75.
- Буторова Л. И., Калинин А. В., Логинов А. Ф. Лекарственные поражения печени. Учебно-методическое пособие для врачей. М., 2010. 64 с.
- DeLeve L. D., Kaplowitz N. Mechanisms of drug-induced liver disease // Gastroenterol Clin N Am. 1995; 24: 787–810.
- Ladas E. J., Kroll D. J., Oberlies N. H. et al. A randomized, controlled, double-blind, pilot study of milk thistle for. the treatment of hepatotoxicity in childhood acute lymphoblastic leukemia (ALL) // Cancer. 2010, Jan 15; 116 (2): 506–513.
- Матвеев А. В., Коняева Е. И., Курченко В. П., Щекатихина А. С. Гепатопротективные свойства силимарина // Клиническая фармакология. 2011, № 2.
М. Л. Бабаян, кандидат медицинских наук А. И. Хавкин, доктор медицинских наук, профессор
ФГБУ «МНИИ педиатрии и детской хирургии» МЗ РФ, Москва
Контактная информация об авторах для переписки
Диагностика и лечение
Если повышена концентрация ферментов, важно установить причину отклонения АСТ и АЛТ от нормы в большую сторону.
Сделать это может только специалист на основании результатов некоторых исследований. Только по биохимическому анализу крови диагностика не выполняется. Врач назначает такие диагностические мероприятия:
- Компьютерная томография;
- Общий анализ крови;
- УЗИ и ЭКГ;
- Биопсия печени, если есть подозрения на патологии этого внутреннего уровня;
- Анализ на уровень железа в крови.
При определении причины повышения концентрации ферментов важно также смотреть на уровень билирубина, щелочной фосфатазы и ГГТП.
Если существуют подозрения на онкологическую патологию злокачественного характера, назначаются исследования на онкомаркеры и другие анализы, помогающие диагностировать рак.

Только определив причины повышения концентрации ферментов в крови, назначается соответствующая терапия. Если лечение дает положительный результат, уровень белков нормализуется.